题目
【实验】配制100mL1.00mol/LNaCl溶液.(1)计算需要NaCl固体的质量: g.(2)根据计算结果,称量NaCl固体.(3)将称好的NaCl固体放入烧杯中,加入适量蒸馏水,用玻璃棒搅拌,使NaCl固体全部溶解.(4)将浇杯中的溶液沿玻璃棒注入100mL容量瓶(如图),并用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,将洗涤液也都注入容量瓶。轻轻摇动容量瓶,使溶液混合均匀.n-|||-100mL-|||-20℃-|||-向容量-|||-瓶中转移溶液(5)将蒸馏水注入容量瓶,当液面离容量瓶颈部的刻度线1sim 2cm时,改用胶头滴管滴加蒸馏水至溶液的凹液面与刻度线相切。盖好瓶塞,反复上下颠倒,摇匀.(6)将配制好的溶液倒入试剂瓶中,并贴好标签. ①aq表示某种物质的水溶液,如NaOH(aq))表示NaOH的水溶液.②为了与容量瓶的精度相匹配,称量固体时应使用分析天平。考虑到学校的实际情况,本实验可暂用托盘天平或普通电子天平代替.n-|||-100mL-|||-20℃-|||-向容量-|||-瓶中转移溶液思考与讨论(1)为什么要用蒸馏水洗涤烧杯内壁和玻璃棒2~3次,并将洗涤液也都注入容量瓶?(2)如果将烧杯中的溶液转移到容量瓶时不慎洒到容量瓶外,最后配成的溶液中溶质的实际浓度比所要求的大了还是小了?(3)如果在读数时,仰视或者俯视容量瓶上的刻度线,最后配成的溶液中溶质的实际浓度比所要求的大了还是小了?
【实验】
配制$100mL1.00mol/LNaCl$溶液.
(1)计算需要$NaCl$固体的质量: $g$.
(2)根据计算结果,称量$NaCl$固$体$.
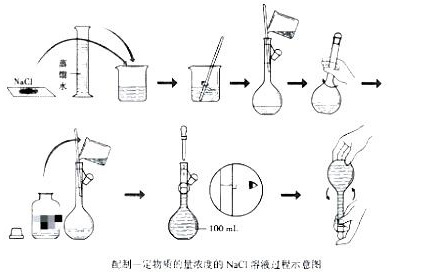
(3)将称好的$NaCl$固体放入烧杯中,加入适量蒸馏水,用玻璃棒搅拌,使$NaCl$固体全部溶解.
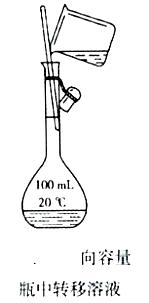
(4)将浇杯中的溶液沿玻璃棒注入$100mL$容量瓶(如图),并用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,将洗
涤液也都注入容量瓶。轻轻摇动容量瓶,使溶液混合均匀.
(5)将蒸馏水注入容量瓶,当液面离容量瓶颈部的刻度线$1\sim 2cm$时,改用胶头滴管滴加蒸馏水至溶液的凹液面与刻度线相切。盖好瓶塞,反复上下颠倒,摇匀.
(6)将配制好的溶液倒入试剂瓶中,并贴好标签.
①aq表示某种物质的水溶液,如$NaOH\left(aq\right)$)表示$NaOH$的水溶液.
②为了与容量瓶的精度相匹配,称量固体时应使用分析天平。考虑到学校的实际情况,本实验可暂用托盘天平或普通电子天平代替.
思考与讨论
(1)为什么要用蒸馏水洗涤烧杯内壁和玻璃棒2~3次,并将洗涤液也都注入容量瓶?
(2)如果将烧杯中的溶液转移到容量瓶时不慎洒到容量瓶外,最后配成的溶液中溶质的实际浓度比所要求的大了还是小了?
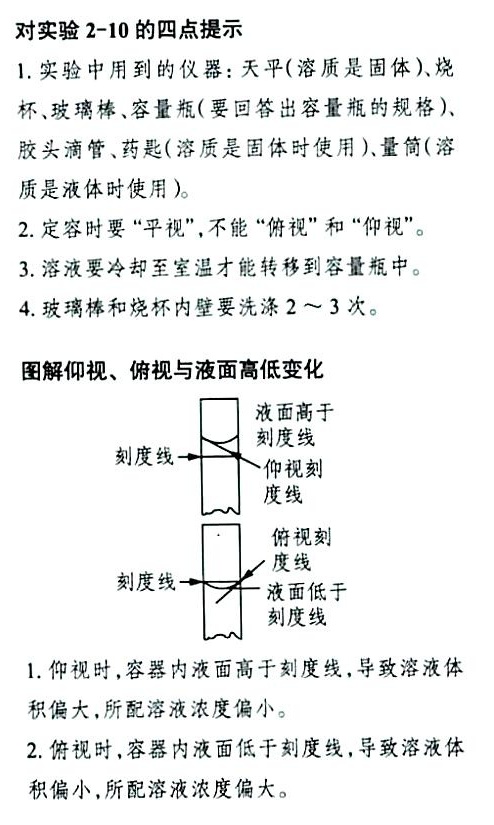
(3)如果在读数时,仰视或者俯视容量瓶上的刻度线,最后配成的溶液中溶质的实际浓度比所要求的大了还是小了?
题目解答
答案