17.将下列过程设计成原电池,并计算298 K时电池的电动势。-|||-(1) ^2+(aq,a=0.5)arrow (Zn)^2+(aq,a=0.1)-|||-(2) _(2)(p=100kpa)arrow (H)_(2)(p=10kpa) kPa)
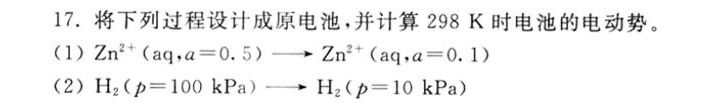
题目解答
答案

解析
考查要点:本题要求设计原电池并计算电动势,涉及浓度变化和压力变化对电极电势的影响,需应用Nernst方程。
解题思路:
- 确定氧化还原反应:负极发生氧化反应,正极发生还原反应。
- 设计半电池:根据反应物状态(溶液浓度或气体压力)设计对应的电极。
- 应用Nernst方程:计算两极电势差,总电动势为两极电势之差。
破题关键:
- 浓度变化:锌离子浓度变化对应金属锌的溶解与沉积。
- 压力变化:氢气压力变化对应氢气的氧化与还原。
- 公式选择:电动势公式需根据反应类型选择正确的活度或压力比。
第(1)题
负极反应
金属锌溶解为低浓度锌离子:
$\text{Zn(s)} \rightarrow 2e^- + \text{Zn}^{2+}(\text{a}=0.1)$
正极反应
高浓度锌离子沉积为金属锌:
$\text{Zn}^{2+}(\text{a}=0.5) + 2e^- \rightarrow \text{Zn(s)}$
电池反应
$\text{Zn}^{2+}(\text{aq, a}=0.5) \rightarrow \text{Zn}^{2+}(\text{aq, a}=0.1)$
电动势计算
标准电极电势 $E^\theta = 0$,根据Nernst方程:
$E = \frac{RT}{2F} \ln \frac{a_{\text{正极}}}{a_{\text{负极}}} = \frac{RT}{2F} \ln \frac{0.5}{0.1} = \frac{RT}{2F} \ln 5$
第(2)题
负极反应
氢气氧化为氢离子:
$\text{H}_2(p=100\ \text{kPa}) \rightarrow 2\text{H}^+ + 2e^-$
正极反应
氢离子还原为氢气:
$2\text{H}^+ + 2e^- \rightarrow \text{H}_2(p=10\ \text{kPa})$
电池反应
$\text{H}_2(p=100\ \text{kPa}) \rightarrow \text{H}_2(p=10\ \text{kPa})$
电动势计算
标准电极电势 $E^\theta = 0$,根据Nernst方程:
$E = \frac{RT}{2F} \ln \frac{p_{\text{负极}}}{p_{\text{正极}}} = \frac{RT}{2F} \ln \frac{100}{10} = \frac{RT}{2F} \ln 10$