将己二酸和己二胺制成尼龙-66盐,然后缩聚制成尼龙-66,反应温度为235℃,平衡常数K=432,问:(1)如封闭体系,最大可达多少?(2)如开放体系并且体系中小分子水的含量为7.2×10-3,求可能达到的反应程度和平均聚合度?(3) 如开放体系,要得到=200的聚合物,体系的水应该控制在多少?
将己二酸和己二胺制成尼龙-66盐,然后缩聚制成尼龙-66,反应温度为235℃,平衡常数K=432,问:
(1)如封闭体系,最大可达多少?
(2)如开放体系并且体系中小分子水的含量为7.2×10-3,求可能达到的反应程度和平均聚合度?
(3) 如开放体系,要得到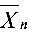 =200的聚合物,体系的水应该控制在多少?
=200的聚合物,体系的水应该控制在多少?
题目解答
答案
解:(1) 封闭体系下,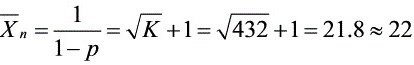
(2) 开放体系下,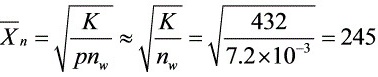
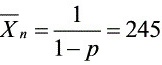
P=0.996
(3) 开放体系下,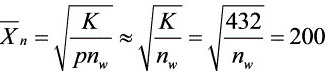
nw=1.08×10-2
解析
考查要点:本题主要考查缩聚反应中封闭体系与开放体系的反应程度及平均聚合度的计算,涉及平衡常数的应用和相关公式的推导。
解题核心思路:
- 封闭体系:反应达到平衡时,通过平衡常数$K$直接计算最大平均聚合度$\overline{X}_n$。
- 开放体系:需考虑小分子副产物(如水)的浓度对反应的影响,通过公式$\overline{X}_n = \sqrt{\dfrac{K}{n_w}}$计算聚合度,并结合反应程度$p$的关系式求解。
破题关键点:
- 封闭体系公式:$\overline{X}_n = \sqrt{K} + 1$。
- 开放体系公式:$\overline{X}_n = \sqrt{\dfrac{K}{n_w}}$,其中$n_w$为小分子水的浓度。
- 反应程度与聚合度关系:$\overline{X}_n = \dfrac{1}{1-p}$。
第(1)题
封闭体系下最大平均聚合度
根据封闭体系的平衡关系,最大平均聚合度公式为:
$\overline{X}_n = \sqrt{K} + 1$
代入$K=432$:
$\overline{X}_n = \sqrt{432} + 1 \approx 21.8 \approx 22$
第(2)题
开放体系下反应程度与平均聚合度
-
计算平均聚合度
开放体系公式为:
$\overline{X}_n = \sqrt{\dfrac{K}{n_w}}$
代入$n_w = 7.2 \times 10^{-3}$:
$\overline{X}_n = \sqrt{\dfrac{432}{7.2 \times 10^{-3}}} = \sqrt{60000} \approx 245$ -
求反应程度$p$
根据$\overline{X}_n = \dfrac{1}{1-p}$,解得:
$1-p = \dfrac{1}{245} \implies p \approx 0.996$
第(3)题
控制水浓度以达到目标聚合度
目标$\overline{X}_m = 200$,代入开放体系公式:
$\overline{X}_n = \sqrt{\dfrac{K}{n_w}} \implies 200 = \sqrt{\dfrac{432}{n_w}}$
解得:
$n_w = \dfrac{432}{200^2} = 1.08 \times 10^{-2}$