27、汽车尾气是造成雾霾天气的重要原因之一,尾气中的主要污染物为CxHy、NO、CO、SO2及固体颗粒物等。研究汽车尾气的成分及其发生的反应,可以为更好的治理汽车尾气提供技术支持。请回答下列问题: (1)汽车尾气净化的主要原理为:2NO(g)+2CO(g)=2CO2 (g)+N2 (g) △H<0。 ①该反应的速率-时间图像如右图中左图所示。若其他条件不变,仅在反应前加人合适的催化剂,则其速率-时间图像如右图中右图所示。 v-|||-a v((正)-|||-b-|||-vx(逆)-|||-o , ,-|||-未加催化.制-|||-v-|||-a: (正)-|||-b,-|||-(逆)-|||-o l3-|||-加催化胡以下说法正确的是(填对应字母)。 A.a1>a2 B.b1<b2 C.t1>t2 D.右图中阴影部分面积更大 E.左图中阴影部分面积更大 (2)活性炭也可用于处理汽车尾气中的NO。在1L 恒容密闭容器中加入0.1000 mol NO 和2.030 mol 固体活性炭,生成A、B两种气体,在不同温度下测得平衡体系中各物质的物质的量以及容器内压强如下表: 活性炭/mol NO/mol A/mol B/mol p/MPa 200℃ 2.000 0.0400 0.0300 0.0300 3.93 335℃ 2.005 0.0500 0.0250 0.0250 p 根据上表数据,写出容器中发生反应的化学方程式________并判断p_____3.93 MPa(用“>” 、“ <"或“=” 填空)。 计算反应体系在200℃时的平衡常数Kp _____________ (用平衡分压代替平衡浓度计算,分压=总压×体积分数)。 (3)汽车尾气中的SO2可用石灰水来吸收,生成亚硫酸钙浊液。常温下,测得某纯CaSO3与水形成的浊液pH为9,已知Kal(H2SO3)=1.8×10-2,Ka2(H2SO3)=6.0×10-9,忽略SO32-的第二步水解,则Ksp(CaSO3)= ______________ 。 (4)尾气中的碳氢化合物含有甲烷,其在排气管的催化转化器中可发生如下反应 CH4(g)+H2O(1)=CO(g)+3H2 (g) △H=+250.1 kJ/mol。已知CO(g)、H2(g)的燃烧热依次为283.0 kJ/mol、285.8 kJ/mol,请写出表示甲烷燃烧热的热化学方程式_________________________________ 。以CH4(g)为燃料可以设计甲烷燃料电池,该电池以稀H2SO4作电解质溶液,其负极电极反应式为__________,已知该电池的能量转换效率为86. 4%,则该电池的比能量为_________kW.h.kg-1(结果保留1位小数,比能量=v-|||-a v((正)-|||-b-|||-vx(逆)-|||-o , ,-|||-未加催化.制-|||-v-|||-a: (正)-|||-b,-|||-(逆)-|||-o l3-|||-加催化胡,1kW·h=3.6×106J) 。
27、汽车尾气是造成雾霾天气的重要原因之一,尾气中的主要污染物为CxHy、NO、CO、SO2及固体颗粒物等。研究汽车尾气的成分及其发生的反应,可以为更好的治理汽车尾气提供技术支持。请回答下列问题:
(1)汽车尾气净化的主要原理为:2NO(g)+2CO(g)=2CO2 (g)+N2 (g) △H<0。
①该反应的速率-时间图像如右图中左图所示。若其他条件不变,仅在反应前加人合适的催化剂,则其速率-时间图像如右图中右图所示。
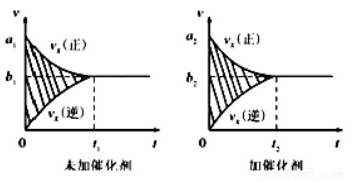
以下说法正确的是(填对应字母)。
A.a1>a2 B.b1<b2 C.t1>t2
D.右图中阴影部分面积更大 E.左图中阴影部分面积更大
(2)活性炭也可用于处理汽车尾气中的NO。在1L 恒容密闭容器中加入0.1000 mol NO 和2.030 mol 固体活性炭,生成A、B两种气体,在不同温度下测得平衡体系中各物质的物质的量以及容器内压强如下表:
活性炭/mol
NO/mol
A/mol
B/mol
p/MPa
200℃
2.000
0.0400
0.0300
0.0300
3.93
335℃
2.005
0.0500
0.0250
0.0250
p
根据上表数据,写出容器中发生反应的化学方程式________并判断p_____3.93 MPa(用“>” 、“ <"或“=” 填空)。
计算反应体系在200℃时的平衡常数Kp _____________ (用平衡分压代替平衡浓度计算,分压=总压×体积分数)。
(3)汽车尾气中的SO2可用石灰水来吸收,生成亚硫酸钙浊液。常温下,测得某纯CaSO3与水形成的浊液pH为9,已知Kal(H2SO3)=1.8×10-2,Ka2(H2SO3)=6.0×10-9,忽略SO32-的第二步水解,则Ksp(CaSO3)= ______________ 。
(4)尾气中的碳氢化合物含有甲烷,其在排气管的催化转化器中可发生如下反应
CH4(g)+H2O(1)=CO(g)+3H2 (g) △H=+250.1 kJ/mol。已知CO(g)、H2(g)的燃烧热依次为283.0 kJ/mol、285.8 kJ/mol,请写出表示甲烷燃烧热的热化学方程式_________________________________ 。以CH4(g)为燃料可以设计甲烷燃料电池,该电池以稀H2SO4作电解质溶液,其负极电极反应式为__________,已知该电池的能量转换效率为86. 4%,则该电池的比能量为_________kW.h.kg-1(结果保留1位小数,比能量=![]() ,1kW·h=3.6×106J) 。
,1kW·h=3.6×106J) 。
题目解答
答案
27、(15 分)(1)BC(2分);
(2)C+2NO![]() N2+CO2(2分);>(1分);0.5625(2分);
N2+CO2(2分);>(1分);0.5625(2分);
(3)4.2×10-9(2分);
(4)CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890.3kJ/mol(2分);
CH4-8e-+2H2O=CO2+8H+(2分);13.4(2分);