“绿水青山就是金山银山”。近年来,绿色发展、生态保护成为中国展示给世界的一张新“名片”。汽车尾气是造成大气污染的重要原因之一,减少氮的氧化物在大气中的排放是环境保护的重要内容之一。请回答下列问题:(1)已知:N2(g)+O2(g)===2NO(g) ΔH1=+180.5 kJ·mol-1C(s)+O2(g)===CO2(g) ΔH2=-393.5 kJ·mol-12C(s)+O2(g)===2CO(g) ΔH3=-221 kJ·mol-1若某反应的平衡常数表达式为K=dfrac (c({N)_(2))cdot (c)^2(C(O)_(2))}({c)^2(NO)cdot (c)^2(CO)},则此反应的热化学方程式为________________________________________________________________________________________________________________________________________________。(2)N2O5在一定条件下可发生分解反应:2N2O5(g)4NO2(g)+O2(g),某温度下向恒容密闭容器中加入一定量N2O5,测得N2O5浓度随时间的变化如下表:t/min12345c(N2O5)/(mol·L-1)1.000.710.500.350.250.17①反应开始时体系压强为p,第2 min时体系压强为p1,则p1∶p=________。2~5 min内用NO2表示的该反应的平均反应速率为________________。②一定温度下,在恒容密闭容器中充入一定量N2O5进行该反应,能判断反应已达到化学平衡状态的是______(填字母)。a.NO2和O2的浓度比保持不变b.容器中压强不再变化c.2v正(NO2)=v逆(N2O5)d.气体的密度保持不变(3)Kp是用反应体系中气体物质的分压来表示的平衡常数,即将K表达式中平衡浓度用平衡分压代替。已知反应:NO2(g)+CO(g)NO(g)+CO2(g),该反应中正反应速率v正=k正·p(NO2)·p(CO),逆反应速率v逆=k逆·p(NO)·p(CO2),其中k正、k逆为速率常数,则Kp=________________(用k正、k逆表示)。(4)如图是密闭反应器中按n(N2)∶n(H2)=1∶3投料后,在200 ℃、400 ℃、600 ℃下,合成NH3反应达到平衡时,混合物中NH3的物质的量分数随压强的变化曲线,已知该反应为放热反应。①曲线a对应的温度是________。②M点对应的H2的转化率是________。(5)工业生产中产生的SO2废气可用如图方法获得H2SO4。写出电解的阳极反应式:________________________________________________________________________。解析:(1)若某反应的平衡常数表达式为K=dfrac (c({N)_(2))cdot (c)^2(C(O)_(2))}({c)^2(NO)cdot (c)^2(CO)},则其化学方程式为2NO(g)+2CO(g)===N2(g)+2CO2(g),将题中3个已知热化学方程式依次编号为①②③,根据盖斯定律,由②×2-①-③,可得:2NO(g)+2CO(g)===N2(g)+2CO2(g) ΔH=(-393.5 kJ·mol-1)×2-(+180.5 kJ·mol-1)-(-221 kJ·mol-1)=-746.5 kJ·mol-1。(2)①根据题表中数据及三段式法有:2N2O5(g)4NO2(g)+O2(g)开始/(mol·L-1) 1.00 0 0转化/(mol·L-1) 0.50 1.00 0.252 min时/(mol·L-1) 0.50 1.00 0.25该反应在恒温恒容条件下发生,反应前后气体的压强之比等于物质的量之比,也等于物质的量浓度之比,所以p1∶p=(0.50+1.00+0.25)∶1.00=7∶4。2~5 min内,v(N2O5)=dfrac (c({N)_(2))cdot (c)^2(C(O)_(2))}({c)^2(NO)cdot (c)^2(CO)}=0.11 mol·L-1·min-1,v(NO2)=2v(N2O5)=0.22 mol·L-1·min-1。②反应过程中NO2和O2的浓度比始终保持不变,a项不能说明反应已经达到化学平衡状态;该反应在反应前后气体分子数不相等,反应过程中容器内压强为变量,容器内压强不再变化可以说明反应已经达到化学平衡状态,b项符合题意;v正(NO2)=2v逆(N2O5)时,正、逆反应速率相等,而2v正(NO2)=v逆(N2O5)时,正、逆反应速率不相等,c项不能说明反应已经达到化学平衡状态;反应物和生成物全为气体,气体总质量不变,而容器恒容,故反应过程中气体密度始终不变,d项不能说明反应已经达到化学平衡状态。(3)Kp=dfrac (c({N)_(2))cdot (c)^2(C(O)_(2))}({c)^2(NO)cdot (c)^2(CO)},v正=k正·p(NO2)·p(CO),v逆=k逆·p(NO)·p(CO2),平衡时正、逆反应速率相等,即k正·p(NO2)·p(CO)=k逆·p(NO)·p(CO2),则dfrac (c({N)_(2))cdot (c)^2(C(O)_(2))}({c)^2(NO)cdot (c)^2(CO)}=,故Kp=。(4)①合成氨反应为放热反应,升高温度,平衡向逆反应方向移动,NH3的产率降低,NH3的物质的量分数减小,曲线a、b、c中,在相同条件下曲线a对应NH3的物质的量分数最高,其反应温度最低,所以曲线a对应的温度为200 ℃。②M点NH3的物质的量分数为60%,设NH3为0.6a mol,则N2、H2共为0.4a mol,因为反应器中按n(N2)∶n(H2)=1∶3投料,故M点时H2为0.3a mol,结合N2(g)+3H2(g)2NH3(g)可知,转化的H2的物质的量为0.9a mol,所以M点对应H2的转化率为dfrac (c({N)_(2))cdot (c)^2(C(O)_(2))}({c)^2(NO)cdot (c)^2(CO)}×100%=75%。(5)由题图可知,在电解池的阳极发生Mn2+转化为MnO2的反应,电极反应式为Mn2++2H2O-2e-===MnO2↓+4H+。
“绿水青山就是金山银山”。近年来,绿色发展、生态保护成为中国展示给世界的一张新“名片”。汽车尾气是造成大气污染的重要原因之一,减少氮的氧化物在大气中的排放是环境保护的重要内容之一。请回答下列问题:
(1)已知:N2(g)+O2(g)===2NO(g) ΔH1=+180.5 kJ·mol-1
C(s)+O2(g)===CO2(g) ΔH2=-393.5 kJ·mol-1
2C(s)+O2(g)===2CO(g) ΔH3=-221 kJ·mol-1
若某反应的平衡常数表达式为K=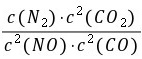 ,则此反应的热化学方程式为
,则此反应的热化学方程式为
________________________________________________________________________
________________________________________________________________________。
(2)N2O5在一定条件下可发生分解反应:2N2O5(g)4NO2(g)+O2(g),某温度下向恒容密闭容器中加入一定量N2O5,测得N2O5浓度随时间的变化如下表:
t/min
1
2
3
4
5
c(N2O5)/(mol·L-1)
1.00
0.71
0.50
0.35
0.25
0.17
①反应开始时体系压强为p,第2 min时体系压强为p1,则p1∶p=________。2~5 min内用NO2表示的该反应的平均反应速率为________________。
②一定温度下,在恒容密闭容器中充入一定量N2O5进行该反应,能判断反应已达到化学平衡状态的是______(填字母)。
a.NO2和O2的浓度比保持不变
b.容器中压强不再变化
c.2v正(NO2)=v逆(N2O5)
d.气体的密度保持不变
(3)Kp是用反应体系中气体物质的分压来表示的平衡常数,即将K表达式中平衡浓度用平衡分压代替。已知反应:NO2(g)+CO(g)NO(g)+CO2(g),该反应中正反应速率v正=k正·p(NO2)·p(CO),逆反应速率v逆=k逆·p(NO)·p(CO2),其中k正、k逆为速率常数,则Kp=________________(用k正、k逆表示)。
(4)如图是密闭反应器中按n(N2)∶n(H2)=1∶3投料后,在200 ℃、400 ℃、600 ℃下,合成NH3反应达到平衡时,混合物中NH3的物质的量分数随压强的变化曲线,已知该反应为放热反应。
①曲线a对应的温度是________。
②M点对应的H2的转化率是________。
(5)工业生产中产生的SO2废气可用如图方法获得H2SO4。写出电解的阳极反应式:________________________________________________________________________。
解析:(1)若某反应的平衡常数表达式为K=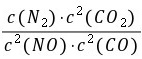 ,则其化学方程式为2NO(g)+2CO(g)===N2(g)+2CO2(g),将题中3个已知热化学方程式依次编号为①②③,根据盖斯定律,由②×2-①-③,可得:2NO(g)+2CO(g)===N2(g)+2CO2(g) ΔH=(-393.5 kJ·mol-1)×2-(+180.5 kJ·mol-1)-(-221 kJ·mol-1)=-746.5 kJ·mol-1。(2)①根据题表中数据及三段式法有:
,则其化学方程式为2NO(g)+2CO(g)===N2(g)+2CO2(g),将题中3个已知热化学方程式依次编号为①②③,根据盖斯定律,由②×2-①-③,可得:2NO(g)+2CO(g)===N2(g)+2CO2(g) ΔH=(-393.5 kJ·mol-1)×2-(+180.5 kJ·mol-1)-(-221 kJ·mol-1)=-746.5 kJ·mol-1。(2)①根据题表中数据及三段式法有:
2N2O5(g)4NO2(g)+O2(g)
开始/(mol·L-1) 1.00 0 0
转化/(mol·L-1) 0.50 1.00 0.25
2 min时/(mol·L-1) 0.50 1.00 0.25
该反应在恒温恒容条件下发生,反应前后气体的压强之比等于物质的量之比,也等于物质的量浓度之比,所以p1∶p=(0.50+1.00+0.25)∶1.00=7∶4。2~5 min内,v(N2O5)=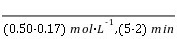 =0.11 mol·L-1·min-1,v(NO2)=2v(N2O5)=0.22 mol·L-1·min-1。②反应过程中NO2和O2的浓度比始终保持不变,a项不能说明反应已经达到化学平衡状态;该反应在反应前后气体分子数不相等,反应过程中容器内压强为变量,容器内压强不再变化可以说明反应已经达到化学平衡状态,b项符合题意;v正(NO2)=2v逆(N2O5)时,正、逆反应速率相等,而2v正(NO2)=v逆(N2O5)时,正、逆反应速率不相等,c项不能说明反应已经达到化学平衡状态;反应物和生成物全为气体,气体总质量不变,而容器恒容,故反应过程中气体密度始终不变,d项不能说明反应已经达到化学平衡状态。(3)Kp=
=0.11 mol·L-1·min-1,v(NO2)=2v(N2O5)=0.22 mol·L-1·min-1。②反应过程中NO2和O2的浓度比始终保持不变,a项不能说明反应已经达到化学平衡状态;该反应在反应前后气体分子数不相等,反应过程中容器内压强为变量,容器内压强不再变化可以说明反应已经达到化学平衡状态,b项符合题意;v正(NO2)=2v逆(N2O5)时,正、逆反应速率相等,而2v正(NO2)=v逆(N2O5)时,正、逆反应速率不相等,c项不能说明反应已经达到化学平衡状态;反应物和生成物全为气体,气体总质量不变,而容器恒容,故反应过程中气体密度始终不变,d项不能说明反应已经达到化学平衡状态。(3)Kp=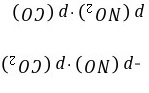 ,v正=k正·p(NO2)·p(CO),v逆=k逆·p(NO)·p(CO2),平衡时正、逆反应速率相等,即k正·p(NO2)·p(CO)=k逆·p(NO)·p(CO2),则
,v正=k正·p(NO2)·p(CO),v逆=k逆·p(NO)·p(CO2),平衡时正、逆反应速率相等,即k正·p(NO2)·p(CO)=k逆·p(NO)·p(CO2),则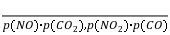 =,故Kp=。(4)①合成氨反应为放热反应,升高温度,平衡向逆反应方向移动,NH3的产率降低,NH3的物质的量分数减小,曲线a、b、c中,在相同条件下曲线a对应NH3的物质的量分数最高,其反应温度最低,所以曲线a对应的温度为200 ℃。②M点NH3的物质的量分数为60%,设NH3为0.6a mol,则N2、H2共为0.4a mol,因为反应器中按n(N2)∶n(H2)=1∶3投料,故M点时H2为0.3a mol,结合N2(g)+3H2(g)2NH3(g)可知,转化的H2的物质的量为0.9a mol,所以M点对应H2的转化率为
=,故Kp=。(4)①合成氨反应为放热反应,升高温度,平衡向逆反应方向移动,NH3的产率降低,NH3的物质的量分数减小,曲线a、b、c中,在相同条件下曲线a对应NH3的物质的量分数最高,其反应温度最低,所以曲线a对应的温度为200 ℃。②M点NH3的物质的量分数为60%,设NH3为0.6a mol,则N2、H2共为0.4a mol,因为反应器中按n(N2)∶n(H2)=1∶3投料,故M点时H2为0.3a mol,结合N2(g)+3H2(g)2NH3(g)可知,转化的H2的物质的量为0.9a mol,所以M点对应H2的转化率为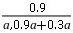 ×100%=75%。(5)由题图可知,在电解池的阳极发生Mn2+转化为MnO2的反应,电极反应式为Mn2++2H2O-2e-===MnO2↓+4H+。
×100%=75%。(5)由题图可知,在电解池的阳极发生Mn2+转化为MnO2的反应,电极反应式为Mn2++2H2O-2e-===MnO2↓+4H+。
题目解答
答案
答案:(1)2NO(g)+2CO(g)===N2(g)+2CO2(g) ΔH=-746.5 kJ·mol-1
(2)①7∶4 0.22 mol·L-1·min-1 ②b
(3)
(4)①200 ℃ ②75%
(5)Mn2++2H2O-2e-===MnO2↓+4H+