题目
已知下列反应在298K时的标准平衡常数①(g)=!=!= (Cl)_(2)(g)+(Br)_(2)(g),(g)=!=!= (Cl)_(2)(g)+(Br)_(2)(g)②(g)=!=!= (Cl)_(2)(g)+(Br)_(2)(g),(g)=!=!= (Cl)_(2)(g)+(Br)_(2)(g)试求该温度时反应③(g)=!=!= (Cl)_(2)(g)+(Br)_(2)(g)的平衡常数(g)=!=!= (Cl)_(2)(g)+(Br)_(2)(g)。
已知下列反应在298K时的标准平衡常数
①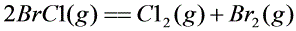 ,
,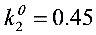
②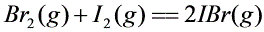 ,
,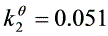
试求该温度时反应③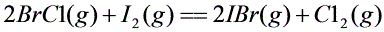 的平衡常数
的平衡常数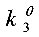 。
。
题目解答
答案
①+②=③
根据多重平衡规则,则有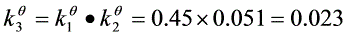
解析
考查要点:本题主要考查化学平衡常数的叠加性质,即多个反应相加时平衡常数相乘的规律。
解题核心思路:
- 反应叠加原理:将已知的两个反应通过相加得到目标反应,注意中间物质的抵消。
- 平衡常数关系:若目标反应是两个反应的简单相加,则其平衡常数为两反应平衡常数的乘积。
破题关键点:
- 正确组合反应式:通过观察反应物与生成物的组成,确定如何将反应①和反应②叠加得到反应③。
- 验证中间物质抵消:确保叠加后中间物质(如Br₂)在总反应中被完全抵消,不参与最终反应式。
反应叠加过程
-
写出已知反应:
- 反应①:$2\text{BrCl}(g) \rightleftharpoons \text{Cl}_2(g) + \text{Br}_2(g)$,$K_1^\theta = 0.45$
- 反应②:$\text{Br}_2(g) + \text{I}_2(g) \rightleftharpoons 2\text{IBr}(g)$,$K_2^\theta = 0.051$
-
叠加反应式:
- 将反应①和反应②相加:
$\begin{align*} 2\text{BrCl} &\rightarrow \text{Cl}_2 + \text{Br}_2 \quad (K_1) \\ \text{Br}_2 + \text{I}_2 &\rightarrow 2\text{IBr} \quad (K_2) \\ \hline 2\text{BrCl} + \text{I}_2 &\rightarrow \text{Cl}_2 + 2\text{IBr} \quad (K_3 = K_1 \cdot K_2) \end{align*}$ - 叠加后$\text{Br}_2$被抵消,最终得到目标反应③。
- 将反应①和反应②相加:
平衡常数计算
根据平衡常数叠加规则:
$K_3^\theta = K_1^\theta \cdot K_2^\theta = 0.45 \times 0.051 = 0.023$