题目
1.25℃时H2O(1)及H2 O(g)的标准摩尔生成焓分别为 -286kJcdot (mol)^-1 及 -242kJcdot (mol)^-1 则水在-|||-25℃时的摩尔气化焓 (Delta )_({Na)_(P)}(H)_(m)= __

题目解答
答案
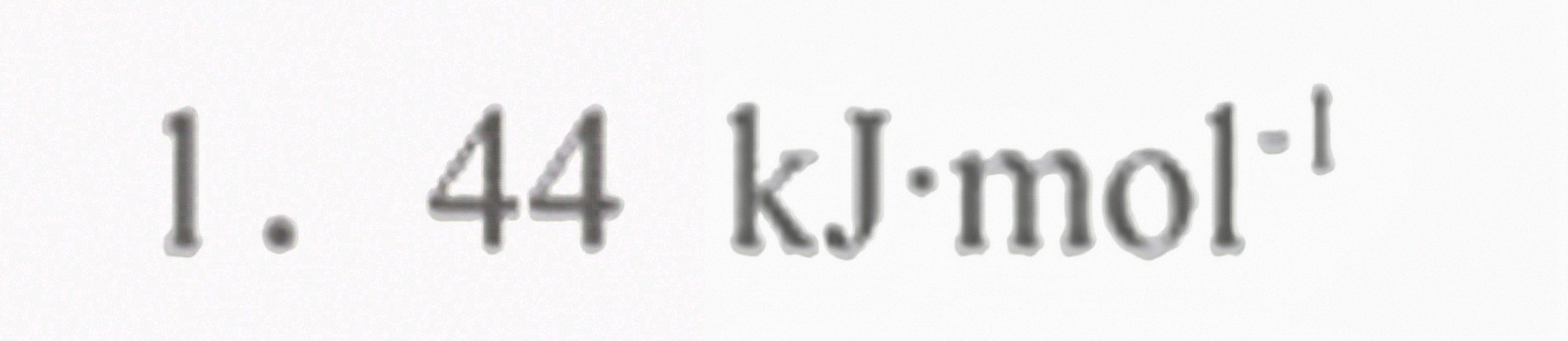
解析
步骤 1:理解摩尔气化焓的定义
摩尔气化焓是指在标准状态下,1摩尔液体完全转化为同温同压下的气体时所吸收的热量。用符号 ${\Delta }_{NaP}{H}_{m}$ 表示。
步骤 2:应用标准摩尔生成焓计算摩尔气化焓
标准摩尔生成焓是指在标准状态下,由稳定单质生成1摩尔物质时的焓变。题目中给出的H2O(1)和H2O(g)的标准摩尔生成焓分别为 $-286kJ\cdot {mol}^{-1}$ 和 $-242kJ\cdot {mol}^{-1}$。摩尔气化焓可以通过以下公式计算:
${\Delta }_{NaP}{H}_{m} = {\Delta }_{f}H_{m}^{(g)} - {\Delta }_{f}H_{m}^{(l)}$
其中,${\Delta }_{f}H_{m}^{(g)}$ 是H2O(g)的标准摩尔生成焓,${\Delta }_{f}H_{m}^{(l)}$ 是H2O(1)的标准摩尔生成焓。
步骤 3:代入数值计算
将题目中给出的数值代入公式中计算:
${\Delta }_{NaP}{H}_{m} = -242kJ\cdot {mol}^{-1} - (-286kJ\cdot {mol}^{-1}) = 44kJ\cdot {mol}^{-1}$
摩尔气化焓是指在标准状态下,1摩尔液体完全转化为同温同压下的气体时所吸收的热量。用符号 ${\Delta }_{NaP}{H}_{m}$ 表示。
步骤 2:应用标准摩尔生成焓计算摩尔气化焓
标准摩尔生成焓是指在标准状态下,由稳定单质生成1摩尔物质时的焓变。题目中给出的H2O(1)和H2O(g)的标准摩尔生成焓分别为 $-286kJ\cdot {mol}^{-1}$ 和 $-242kJ\cdot {mol}^{-1}$。摩尔气化焓可以通过以下公式计算:
${\Delta }_{NaP}{H}_{m} = {\Delta }_{f}H_{m}^{(g)} - {\Delta }_{f}H_{m}^{(l)}$
其中,${\Delta }_{f}H_{m}^{(g)}$ 是H2O(g)的标准摩尔生成焓,${\Delta }_{f}H_{m}^{(l)}$ 是H2O(1)的标准摩尔生成焓。
步骤 3:代入数值计算
将题目中给出的数值代入公式中计算:
${\Delta }_{NaP}{H}_{m} = -242kJ\cdot {mol}^{-1} - (-286kJ\cdot {mol}^{-1}) = 44kJ\cdot {mol}^{-1}$