胺的制法制取胺的方法主要有:用氨做亲核试剂进行亲核取代反应;含氮化合物的还原。(1)氨的烃基化① 在一定压力下,将卤代烃与氨溶液共热,卤代烃与氨发生亲核取代反应,通常反应的最后产物是一级、二级、三级胺和季铵盐的混合物。② 芳环上卤素邻、对位有硝基等强拉电子基团存在时,易发生亲核取代反应。Cl NH-|||-_(2)N (O)_(2)+2N(H)_(3)- 一 O2N- - -N(O)_(2)+N(H)_(4)Cl-|||-NO2 NO2③ 卤代芳烃的氨解A. 卤代芳烃在液态氨中能与强碱KNH2(或NaNH2)作用生成苯胺。 B. Cl NH-|||-_(2)N (O)_(2)+2N(H)_(3)- 一 O2N- - -N(O)_(2)+N(H)_(4)Cl-|||-NO2 NO2 C. 反应历程 D. 反应为消除—加成历程,中间体为苯炔。反应历程为: E. Cl NH-|||-_(2)N (O)_(2)+2N(H)_(3)- 一 O2N- - -N(O)_(2)+N(H)_(4)Cl-|||-NO2 NO2 F. NaNH2作用,只得到间位三氟甲基苯胺。 G. Cl NH-|||-_(2)N (O)_(2)+2N(H)_(3)- 一 O2N- - -N(O)_(2)+N(H)_(4)Cl-|||-NO2 NO2 反应也是按消除-加成历程进行的: 第一步:生成苯炔。 Cl NH-|||-_(2)N (O)_(2)+2N(H)_(3)- 一 O2N- - -N(O)_(2)+N(H)_(4)Cl-|||-NO2 NO2 ⏺ 第二步:苯炔与氨离子的加成可能生成(3)(4)两种碳负离子,(4)比(3)稳定。 Cl NH-|||-_(2)N (O)_(2)+2N(H)_(3)- 一 O2N- - -N(O)_(2)+N(H)_(4)Cl-|||-NO2 NO2 (2)含氮化合物的还原 ① 硝基化合物的还原—芳胺的制取。 催化加氢:常用的催化剂是镍、铂、钯等。 Cl NH-|||-_(2)N (O)_(2)+2N(H)_(3)- 一 O2N- - -N(O)_(2)+N(H)_(4)Cl-|||-NO2 NO2 化学还原:常用的还原剂为铁、锡或氯化亚锡加盐酸,或硫酸,或者醋酸。 Cl NH-|||-_(2)N (O)_(2)+2N(H)_(3)- 一 O2N- - -N(O)_(2)+N(H)_(4)Cl-|||-NO2 NO2Cl NH-|||-_(2)N (O)_(2)+2N(H)_(3)- 一 O2N- - -N(O)_(2)+N(H)_(4)Cl-|||-NO2 NO2 Na2S,NaSH,(NH4)2S的水溶液等选择性还原剂即可达到目的。 Cl NH-|||-_(2)N (O)_(2)+2N(H)_(3)- 一 O2N- - -N(O)_(2)+N(H)_(4)Cl-|||-NO2 NO2 α-萘胺和β-萘胺的合成 α-萘胺可由α-硝基萘还原制得。 Cl NH-|||-_(2)N (O)_(2)+2N(H)_(3)- 一 O2N- - -N(O)_(2)+N(H)_(4)Cl-|||-NO2 NO2 但β-硝基萘不易得到,因此β-萘胺不能由β-硝基萘的还原制取。需用间接方法制取。 Cl NH-|||-_(2)N (O)_(2)+2N(H)_(3)- 一 O2N- - -N(O)_(2)+N(H)_(4)Cl-|||-NO2 NO2 -N键化合物的还原 腈、肟、酰胺等含氮化合物,都可以还原为胺。腈和肟被还原为一级胺,酰胺则可被还原为各级胺。 腈的还原 ⏺ 腈在乙醇中与金属钠作用还原成一级胺: RC≡N + 4C2H5OH + 4Na → RCH2NH2 + 4C2H5ONa 腈催化加氢还原得到一级胺,同时产生少量的二级和三级胺。 Cl NH-|||-_(2)N (O)_(2)+2N(H)_(3)- 一 O2N- - -N(O)_(2)+N(H)_(4)Cl-|||-NO2 NO2 用氢化铝锂做还原剂,则不会生成二级和三级胺,反应在无水乙醚或四氢呋喃中进行,反应产物水解得胺。 Cl NH-|||-_(2)N (O)_(2)+2N(H)_(3)- 一 O2N- - -N(O)_(2)+N(H)_(4)Cl-|||-NO2 NO2 酰胺的还原 Cl NH-|||-_(2)N (O)_(2)+2N(H)_(3)- 一 O2N- - -N(O)_(2)+N(H)_(4)Cl-|||-NO2 NO2 (3)还原氨化 ① 酮或醛与氨作用,在氢和适当的催化剂存在下,转变为一级胺。 Cl NH-|||-_(2)N (O)_(2)+2N(H)_(3)- 一 O2N- - -N(O)_(2)+N(H)_(4)Cl-|||-NO2 NO2 ② 若以一级、二级胺代替氨,则可生成二级、三级胺: Cl NH-|||-_(2)N (O)_(2)+2N(H)_(3)- 一 O2N- - -N(O)_(2)+N(H)_(4)Cl-|||-NO2 NO2 abriel)合成法—合成伯胺 Cl NH-|||-_(2)N (O)_(2)+2N(H)_(3)- 一 O2N- - -N(O)_(2)+N(H)_(4)Cl-|||-NO2 NO2
胺的制法
制取胺的方法主要有:用氨做亲核试剂进行亲核取代反应;含氮化合物的还原。
(1)氨的烃基化
① 在一定压力下,将卤代烃与氨溶液共热,卤代烃与氨发生亲核取代反应,通常反应的最后产物是一级、二级、三级胺和季铵盐的混合物。
② 芳环上卤素邻、对位有硝基等强拉电子基团存在时,易发生亲核取代反应。
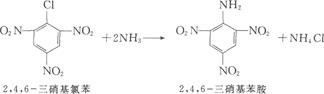
③ 卤代芳烃的氨解
A. 卤代芳烃在液态氨中能与强碱KNH2(或NaNH2)作用生成苯胺。B.
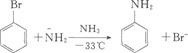
C. 反应历程
D. 反应为消除—加成历程,中间体为苯炔。反应历程为:
E.
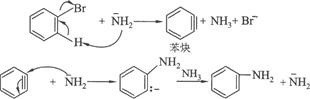
F. NaNH2作用,只得到间位三氟甲基苯胺。
G.
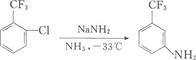
反应也是按消除-加成历程进行的: 第一步:生成苯炔。
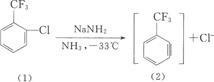
⏺
第二步:苯炔与氨离子的加成可能生成(3)(4)两种碳负离子,(4)比(3)稳定。
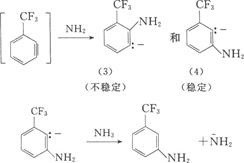
(2)含氮化合物的还原
① 硝基化合物的还原—芳胺的制取。
催化加氢:常用的催化剂是镍、铂、钯等。
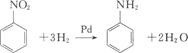
化学还原:常用的还原剂为铁、锡或氯化亚锡加盐酸,或硫酸,或者醋酸。
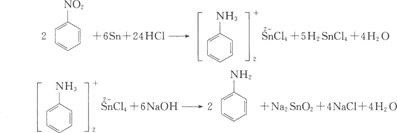
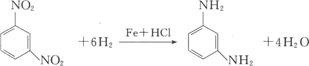
Na2S,NaSH,(NH4)2S的水溶液等选择性还原剂即可达到目的。
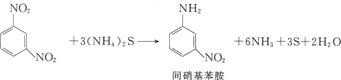
α-萘胺和β-萘胺的合成
α-萘胺可由α-硝基萘还原制得。
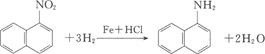
但β-硝基萘不易得到,因此β-萘胺不能由β-硝基萘的还原制取。需用间接方法制取。
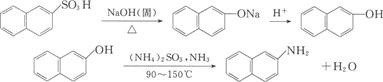
-N键化合物的还原
腈、肟、酰胺等含氮化合物,都可以还原为胺。腈和肟被还原为一级胺,酰胺则可被还原为各级胺。
腈的还原
⏺
腈在乙醇中与金属钠作用还原成一级胺:
RC≡N + 4C2H5OH + 4Na → RCH2NH2 + 4C2H5ONa
腈催化加氢还原得到一级胺,同时产生少量的二级和三级胺。
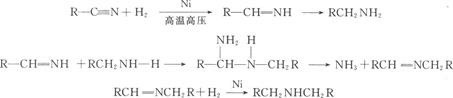
用氢化铝锂做还原剂,则不会生成二级和三级胺,反应在无水乙醚或四氢呋喃中进行,反应产物水解得胺。
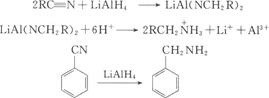
酰胺的还原
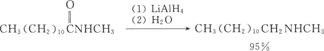
(3)还原氨化
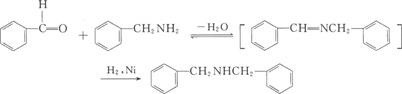
① 酮或醛与氨作用,在氢和适当的催化剂存在下,转变为一级胺。
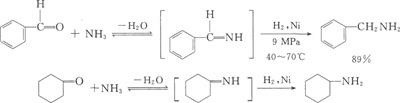
② 若以一级、二级胺代替氨,则可生成二级、三级胺:
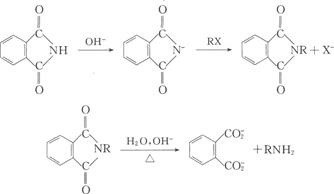
abriel)合成法—合成伯胺
题目解答
答案
a. 卤代芳烃在液态氨中能与强碱 KNH 2 (或 NaNH 2 )作用生成苯胺。 b. 反应历程 反应为消除 — 加成历程,中间体为苯炔。反应历程为: c. 三氟甲基氯苯与 NaNH 2 作用,只得到间位三氟甲基苯胺。 反应也是按消除 - 加成历程进行的: 第一步:生成苯炔。 第二步:苯炔与氨离子的加成可能生成( 3 )( 4 )两种碳负离子,( 4 )比( 3 )稳定。 (2) 含氮化合物的还原 ① 硝基化合物的还原 — 芳胺的制取。 a. 催化加氢:常用的催化剂是镍、铂、钯等。 b. 化学还原:常用的还原剂为铁、锡或氯化亚锡加盐酸,或硫酸,或者醋酸。 c. 二硝基化合物的选择性还原:使用 Na 2 S,NaSH,(NH 4 ) 2 S 的水溶液等选择性还原剂即可达到目的。 d. α- 萘胺和 β- 萘胺的合成 α- 萘胺可由 α- 硝基萘还原制得。 但 β- 硝基萘不易得到,因此 β- 萘胺不能由 β- 硝基萘的还原制取。需用间接方法制取。 ② C-N 键化合物的还原 腈、肟、酰胺等含氮化合物,都可以还原为胺。腈和肟被还原为一级胺,酰胺则可被还原为各级胺。 a. 腈的还原 腈在乙醇中与金属钠作用还原成一级胺: RC≡N + 4C 2 H 5 OH + 4Na → RCH 2 NH 2 + 4C 2 H 5 ONa 腈催化加氢还原得到一级胺,同时产生少量的二级和三级胺。 用氢化铝锂做还原剂,则不会生成二级和三级胺,反应在无水乙醚或四氢呋喃中进行,反应产物水解得胺。 b. 酰胺的还原 (3) 还原氨化 ① 酮或醛与氨作用,在氢和适当的催化剂存在下,转变为一级胺。 ② 若以一级、二级胺代替氨,则可生成二级、三级胺: (4) 加布里埃尔( Gabriel )合成法 — 合成伯胺