题目
a-|||-分水器 置-|||-∠.-|||-(梨形) (球形)-|||-图I:分水回洗装置 图II:分液漏斗实验室制备乙酸正丁酯的化学方程式:CH3COOH+CH3CH2CH2OH⇌_(△)^H_(2SO_{4)}CH3COOCH2CH2CH2CH3+H2O制备过程中还可能的副反应有:CH3CH2CH2CH2OH⇌_(△)^浓H_(2SO_{4)}CH3CH2CH2CH2CH2CH2CH3+H2O主要实验步骤如下:①在干燥的圆底烧瓶中加11.5mL正丁醇、7.2mL冰醋酸和3~4滴浓H2SO4,摇匀后,加几粒沸石,再如图Ⅰ装置安装好分水器、冷凝管.然后小火加热.②将烧瓶中反应后的混合物冷却与分水器中的酯层合并,转入分液漏斗,③依次用10mL水,10mL 10%碳酸钠溶液洗至无酸性(pH=7),再水洗一次,用少许无水硫酸镁干燥.④将干燥后的乙酸正丁酯转入50mL蒸馏烧瓶中,加几粒沸石进行常压蒸馏,收集产品.主要试剂及产物的物理常数: 化合物 正丁醇 冰醋酸 乙酸正丁酯 正丁醚 密度(g•cm-3) 0.810 1.049 0.882 0.7689 沸点(℃) 118.0 118.1 126.1 142 根据以上信息回答下列问题.(1)图I装置中冷水应从 ____ (填a或b),管口通入,反应混合物冷凝回流,通过分水器下端旋塞分出的生成物是 ____ ,其目的是 ____ .(2)在步骤①④中都用到沸石防暴沸,下列关于沸石的说法正确的是 ____ .A.实验室沸石也可用碎瓷片等代替B.如果忘加沸石,可速将沸石加至将近沸腾的液体中C.当重新进行蒸馏时,用过的沸石可继续使用D.沸石为多孔性物质,可使液体平稳地沸腾(3)在步骤③分液时,应选择图II装置中 ____ 形分液漏斗,其原因是 ____ .(4)在提纯粗产品的过程中,用碳酸钠溶液洗涤主要除去的杂质 ____ .若改用氢氧化钠溶液是否可以 ____ (填“可以”或“不可以”),其原因 ____ .(5)步骤④的常压蒸馏,需收集 ____ ℃的馏分,沸点大于140℃的有机化合物的蒸馏,一般不用上述冷凝管而用空气冷凝管,可能原因是 ____ .
 实验室制备乙酸正丁酯的化学方程式:
实验室制备乙酸正丁酯的化学方程式:CH3COOH+CH3CH2CH2OH$⇌_{△}^{H_{2}SO_{4}}$CH3COOCH2CH2CH2CH3+H2O
制备过程中还可能的副反应有:
CH3CH2CH2CH2OH$⇌_{△}^{浓H_{2}SO_{4}}$CH3CH2CH2CH2CH2CH2CH3+H2O
主要实验步骤如下:
①在干燥的圆底烧瓶中加11.5mL正丁醇、7.2mL冰醋酸和3~4滴浓H2SO4,摇匀后,加几粒沸石,再如图Ⅰ装置安装好分水器、冷凝管.然后小火加热.
②将烧瓶中反应后的混合物冷却与分水器中的酯层合并,转入分液漏斗,
③依次用10mL水,10mL 10%碳酸钠溶液洗至无酸性(pH=7),再水洗一次,用少许无水硫酸镁干燥.
④将干燥后的乙酸正丁酯转入50mL蒸馏烧瓶中,加几粒沸石进行常压蒸馏,收集产品.主要试剂及产物的物理常数:
| 化合物 | 正丁醇 | 冰醋酸 | 乙酸正丁酯 | 正丁醚 |
| 密度(g•cm-3) | 0.810 | 1.049 | 0.882 | 0.7689 |
| 沸点(℃) | 118.0 | 118.1 | 126.1 | 142 |
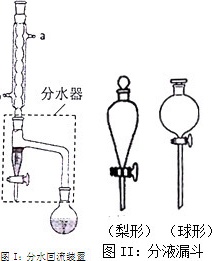
(1)图I装置中冷水应从 ____ (填a或b),管口通入,反应混合物冷凝回流,通过分水器下端旋塞分出的生成物是 ____ ,其目的是 ____ .
(2)在步骤①④中都用到沸石防暴沸,下列关于沸石的说法正确的是 ____ .
A.实验室沸石也可用碎瓷片等代替
B.如果忘加沸石,可速将沸石加至将近沸腾的液体中
C.当重新进行蒸馏时,用过的沸石可继续使用
D.沸石为多孔性物质,可使液体平稳地沸腾
(3)在步骤③分液时,应选择图II装置中 ____ 形分液漏斗,其原因是 ____ .
(4)在提纯粗产品的过程中,用碳酸钠溶液洗涤主要除去的杂质 ____ .若改用氢氧化钠溶液是否可以 ____ (填“可以”或“不可以”),其原因 ____ .
(5)步骤④的常压蒸馏,需收集 ____ ℃的馏分,沸点大于140℃的有机化合物的蒸馏,一般不用上述冷凝管而用空气冷凝管,可能原因是 ____ .
题目解答
答案
解:(1)冷水从下进上出冷凝效果最好;水的密度比乙酸正丁酯大;将水分离使平衡正向移动,提高反应产率,
故答案为:b;水;分离酯化反应生成的水,使平衡正向移动,提高反应产率;
(2)A.沸石为多孔性物质,可用碎瓷片等代替,故A正确;
B.如果忘加沸石,将沸石加至将近沸腾的液体中,可能引起液体飞溅,故B错误;
C.使用过一次后,空气几乎排尽,被液体填充,不再具有提供汽化中心的效果,故C错误;
D.沸石的工作原理是提供汽化中心,汽化中心的来源是沸石多孔结构中包含的空气.这些空气在加热后膨胀,形成气泡溢出,成为了汽化中心,故D正确.
故选:AD;
(3)梨形分液漏斗靠近旋塞处比较细长,分离操作更容易,故答案为:梨;梨形分液漏斗靠近旋塞处比较细长,双液界面更清晰,分离更完全;
(4)乙酸、硫酸、正丁醇易溶于碳酸钠溶液,且乙酸正丁酯在碳酸钠溶液的溶解度较小;乙酸正丁酯在碱性条件下能发生水解,故答案为:乙酸、硫酸、正丁醇;不可以;用氢氧化钠溶液会使乙酸正丁酯发生水解;
(5)乙酸正丁酯的沸点是126.1度,需收集126.1℃的馏分;水冷凝管温度较低,温差过大,冷凝管会炸裂,故答案为:126.1;防止因温差过大,冷凝管炸裂.
故答案为:b;水;分离酯化反应生成的水,使平衡正向移动,提高反应产率;
(2)A.沸石为多孔性物质,可用碎瓷片等代替,故A正确;
B.如果忘加沸石,将沸石加至将近沸腾的液体中,可能引起液体飞溅,故B错误;
C.使用过一次后,空气几乎排尽,被液体填充,不再具有提供汽化中心的效果,故C错误;
D.沸石的工作原理是提供汽化中心,汽化中心的来源是沸石多孔结构中包含的空气.这些空气在加热后膨胀,形成气泡溢出,成为了汽化中心,故D正确.
故选:AD;
(3)梨形分液漏斗靠近旋塞处比较细长,分离操作更容易,故答案为:梨;梨形分液漏斗靠近旋塞处比较细长,双液界面更清晰,分离更完全;
(4)乙酸、硫酸、正丁醇易溶于碳酸钠溶液,且乙酸正丁酯在碳酸钠溶液的溶解度较小;乙酸正丁酯在碱性条件下能发生水解,故答案为:乙酸、硫酸、正丁醇;不可以;用氢氧化钠溶液会使乙酸正丁酯发生水解;
(5)乙酸正丁酯的沸点是126.1度,需收集126.1℃的馏分;水冷凝管温度较低,温差过大,冷凝管会炸裂,故答案为:126.1;防止因温差过大,冷凝管炸裂.
解析
本题考查乙酸正丁酯制备实验中的关键步骤和原理,涉及分水器冷凝方向、沸石作用、分液漏斗选择、洗涤剂除杂及蒸馏温度控制。解题核心在于:
- 分水器冷凝水方向由下而上,确保冷凝效果;
- 沸石需理解其结构与防暴沸原理;
- 分液漏斗形状与液体分层效果的关系;
- 碳酸钠洗涤的作用及不可用氢氧化钠的原因;
- 蒸馏温度需匹配产物沸点,冷凝管选型需考虑温差。
(1)分水器冷凝方向与分离物质
冷水方向
分水器冷凝管需冷水从下端(b)通入,形成逆流冷凝,冷凝效果最佳。
分离物质
分水器下端旋塞分出的物质是水,因水密度大于乙酸正丁酯,会沉降至分水器底部。
目的
通过及时移除生成水,使酯化反应平衡右移,提高产率。
(2)沸石的选择
选项分析
- A正确:碎瓷片可替代沸石,均能提供汽化中心。
- B错误:未沸腾时加沸石易引发暴沸。
- C错误:用过的沸石孔隙被液体填充,失效。
- D正确:沸石多孔结构释放空气,形成稳定汽化中心。
(3)分液漏斗形状选择
形状选择
应选梨形分液漏斗,因其靠近旋塞处细长,双液界面清晰,分液更彻底。
(4)洗涤剂作用与选择
除去杂质
碳酸钠溶液可中和乙酸、中和硫酸,并溶解正丁醇(与水混溶)。
不能用氢氧化钠
乙酸正丁酯在碱性条件下会发生水解反应,导致产品损失。
(5)蒸馏温度与冷凝管
收集温度
乙酸正丁酯沸点为126.1℃,需收集此温度馏分。
冷凝管选型
沸点>140℃时改用空气冷凝管,因水冷凝管温差大易炸裂。