4.16 一溶液中 (S{O)_(4)}^2- 及 (C{O)_(3)}^2- 的浓度均为 .10molcdot (dm)^-3 ,向其中逐滴加入 ^2+ 溶液。-|||-试通过计算说明:-|||-(1)哪种离子先沉淀?-|||-(2)两种离子的浓度达到何种比例时才能同时沉淀?-|||-(3)开始同时沉淀时,先沉淀的离子浓度为多少?-|||-已知BaSO4的 _(sp)=1.08times (10)^-10 ,BaCO3的 _(sp)=2.58times (10)^-9 。

题目解答
答案
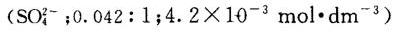
解析
本题考查难溶电解质的溶解平衡以及沉淀先后顺序的判断,解题思路是根据溶度积常数分别计算出开始沉淀时所需离子的浓度,通过比较浓度大小判断沉淀先后顺序,再根据沉淀同时的条件计算离子浓度比例和先沉淀离子的剩余浓度。
(1)判断哪种离子先沉淀
根据溶度积常数$K_{sp}$的表达式,对于$BaSO_{4}$,$K_{sp} = [Ba^{2 + }][SO_{4}^{2 - }]$,开始沉淀时所需$[Ba^{2 + }]$的浓度为:
$[Ba^{2 + }]_{1}=\frac{K_{sp}(BaSO_{4})}{[SO_{4}^{2 - }]}=\frac{1.08\times 10^{-10}}{0.10}=1.08\times 10^{-9}mol\cdot dm^{-3}$
对于$BaCO_{3}$,$K_{sp} = [Ba^{2 + }][CO_{3}^{2 - }]$,开始沉淀时所需$[Ba^{2 + }]$的浓度为:
$[Ba^{2 + }]_{2}=\frac{K_{sp}(BaCO_{3})}{[CO_{3}^{2 - }]}=\frac{2.58\times 10^{-9}}{0.10}=2.58\times 10^{-8}mol\cdot dm^{-3}$
因为$[Ba^{2 + }]_{1}<[Ba^{2 + }]_{2}$,所以$SO_{4}^{2 - }$先沉淀。
(2)计算两种离子的浓度达到何种比例时才能同时沉淀
当两种离子同时沉淀时,$[Ba^{2 + }]$满足$K_{sp}(BaSO_{4}) = [Ba^{2 + }][SO_{4}^{2 - }]$和$K_{sp}(BaCO_{3}) = [Ba^{2 + }][CO_{3}^{2 - }]$,则有:
$\frac{K_{sp}(BaSO_{4})}{[SO_{4}^{2 - }]}=\frac{K_{sp}(BaCO_{3})}{[CO_{3}^{2 - }]}$
$\frac{[SO_{4}^{2 - }]}{[CO_{3}^{2 - }]}=\frac{K_{sp}(BaSO_{4})}{K_{sp}(BaCO_{3})}=\frac{1.08\times 10^{-10}}{2.58\times 10^{-9}} = 0.042:1$
(3)计算开始同时沉淀时,先沉淀的离子浓度为多少
开始同时沉淀时,$[Ba^{2 + }]$满足$K_{sp}(BaSO_{4}) = [Ba^{2 + }][SO_{4}^{2 - }]$,此时$[Ba^{2 + }]=\frac{K_{sp}(BaSO_{4})}{[SO_{4}^{2 - }]}$,而$[SO_{4}^{2 - }]$与$[CO_{3}^{2 - }]$满足$\frac{[SO_{4}^{2 - }]}{[CO_{3}^{2 - }]} = 0.042:1$,$[CO_{3}^{2 - }]=0.10mol\cdot dm^{-3}$,则$[SO_{4}^{2 - }]=0.042\times0.10 = 4.2\times 10^{-3}mol\cdot dm^{-3}$。