题目
(10)3的间歇釜中进行均相反应A + B → P,为防止产物P在高温分解,反应维持在75℃等温操作,-(r)_(A)=k(C)_(A)(C)_(B)kmol/Lcdot S,-(r)_(A)=k(C)_(A)(C)_(B)kmol/Lcdot S,活化能-(r)_(A)=k(C)_(A)(C)_(B)kmol/Lcdot S。当反应物A和B的初始浓度均为-(r)_(A)=k(C)_(A)(C)_(B)kmol/Lcdot S,A的转化率-(r)_(A)=k(C)_(A)(C)_(B)kmol/Lcdot S时,该间歇釜平均每分钟可处理0.684kmol的反应物A。今若把反应移到一个管内径为125mm的理想管式反应器中进行,若将温度提升到85℃等温操作,且处理量与所要求达到的转化率均与间歇反应时相同,求所需的管式反应器长度。
(10)
3的间歇釜中进行均相反应A + B → P,为防止产物P在高温分解,反应维持在75℃等温操作,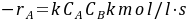 ,
,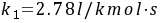 ,活化能
,活化能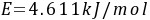 。当反应物A和B的初始浓度均为
。当反应物A和B的初始浓度均为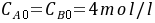 ,A的转化率
,A的转化率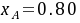 时,该间歇釜平均每分钟可处理0.684kmol的反应物A。今若把反应移到一个管内径为125mm的理想管式反应器中进行,若将温度提升到85℃等温操作,且处理量与所要求达到的转化率均与间歇反应时相同,求所需的管式反应器长度。
时,该间歇釜平均每分钟可处理0.684kmol的反应物A。今若把反应移到一个管内径为125mm的理想管式反应器中进行,若将温度提升到85℃等温操作,且处理量与所要求达到的转化率均与间歇反应时相同,求所需的管式反应器长度。
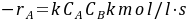 ,
,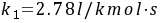 ,活化能
,活化能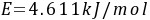 。当反应物A和B的初始浓度均为
。当反应物A和B的初始浓度均为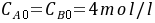 ,A的转化率
,A的转化率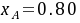 时,该间歇釜平均每分钟可处理0.684kmol的反应物A。今若把反应移到一个管内径为125mm的理想管式反应器中进行,若将温度提升到85℃等温操作,且处理量与所要求达到的转化率均与间歇反应时相同,求所需的管式反应器长度。
时,该间歇釜平均每分钟可处理0.684kmol的反应物A。今若把反应移到一个管内径为125mm的理想管式反应器中进行,若将温度提升到85℃等温操作,且处理量与所要求达到的转化率均与间歇反应时相同,求所需的管式反应器长度。题目解答
答案
(10)
解:根据阿累尼乌斯公式
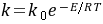 ①分
①分故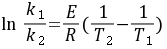 ①分
①分
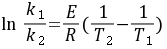 ①分
①分求得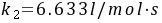 ①分
①分
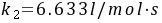 ①分
①分因为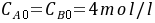 ,且为等摩尔反应,故
,且为等摩尔反应,故
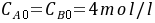 ,且为等摩尔反应,故
,且为等摩尔反应,故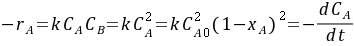 ①分
①分在间歇反应器中所需的反应时间为:
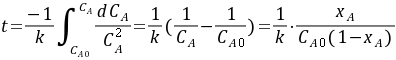 ①分
①分带入得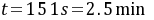 ①分
①分
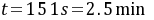 ①分
①分此反应时间应等于在理想管式反应器中的停留时间,即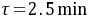 ①分
①分
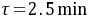 ①分
①分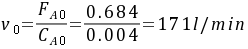 ①分
①分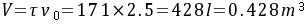 ①分
①分管长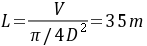 ①分
①分
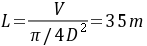 ①分
①分解析
本题主要考查化学反应工程中间歇釜和管式反应器的相关知识,解题思路是先根据阿累尼乌斯公式求出不同温度下的反应速率常数,再计算间歇釜中达到指定转化率所需的反应时间,此时间即为管式反应器的停留时间,接着根据处理量求出进料体积流量,进而得到管式反应器的体积,最后根据管式反应器的体积和管径计算出所需的长度。
- 计算$85^{\circ}C$时的反应速率常数$k_2$
- 已知阿累尼乌斯公式$k = k_0e^{-\frac{E}{RT}}$,对于两个不同温度$T_1$和$T_2$,有$\ln\frac{k_1}{k_2}=\frac{E}{R}(\frac{1}{T_2}-\frac{1}{T_1})$。
- 已知$T_1 = 75^{\circ}C=(75 + 273.15)K = 348.15K$,$k_1 = 2.78L/(kmol\cdot s)$,$E = 4.611\times10^3J/mol$,$R = 8.314J/(mol\cdot K)$,$T_2 = 85^{\circ}C=(85 + 273.15)K = 358.15K$。
- 将上述数据代入$\ln\frac{k_1}{k_2}=\frac{E}{R}(\frac{1}{T_2}-\frac{1}{T_1})$可得:
$\ln\frac{2.78}{k_2}=\frac{4.611\times10^3}{8.314}(\frac{1}{358.15}-\frac{1}{348.15})$
$\ln\frac{2.78}{k_2}=554.61\times(\frac{348.15 - 358.15}{358.15\times348.15})$
$\ln\frac{2.78}{k_2}=554.61\times\frac{-10}{358.15\times348.15}$
$\ln\frac{2.78}{k_2}\approx - 0.47$
$\frac{2.78}{k_2}=e^{-0.47}$
$k_2=\frac{2.78}{e^{-0.47}}\approx 6.633L/(kmol\cdot s)$
- 计算间歇釜中达到$X_A = 0.80$所需的反应时间$t$
- 因为$C_{A0}=C_{B0}=4mol/L$,且为等摩尔反应,所以$-r_A = kC_AC_B = kC_A^2 = kC_{A0}^2(1 - X_A)^2=-\frac{dC_A}{dt}$。
- 对$-r_A = kC_{A0}^2(1 - X_A)^2=-\frac{dC_A}{dt}$进行积分,$C_A = C_{A0}(1 - X_A)$,$dC_A=-C_{A0}dX_A$,则$kC_{A0}^2(1 - X_A)^2=\frac{C_{A0}dX_A}{dt}$,即$dt=\frac{1}{kC_{A0}(1 - X_A)^2}dX_A$。
- 从$X_A = 0$到$X_A = 0.8$积分可得:
$t=\int_{0}^{0.8}\frac{1}{kC_{A0}(1 - X_A)^2}dX_A=\frac{1}{kC_{A0}}\int_{0}^{0.8}\frac{1}{(1 - X_A)^2}dX_A$
令$u = 1 - X_A$,$du=-dX_A$,当$X_A = 0$时,$u = 1$;当$X_A = 0.8$时,$u = 0.2$。
则$t=\frac{1}{kC_{A0}}\int_{1}^{0.2}-\frac{1}{u^2}du=\frac{1}{kC_{A0}}\int_{0.2}^{1}\frac{1}{u^2}du$
$t=\frac{1}{kC_{A0}}[-\frac{1}{u}]_{0.2}^{1}=\frac{1}{kC_{A0}}(-1+\frac{1}{0.2})=\frac{1}{kC_{A0}}\times4=\frac{X_A}{kC_{A0}(1 - X_A)}$ - 代入$k = 6.633L/(kmol\cdot s)$,$C_{A0}=4kmol/m^3$,$X_A = 0.8$可得:
$t=\frac{0.8}{6.633\times4\times(1 - 0.8)}s\approx 151s = 2.5min$
- 计算管式反应器的体积$V$
- 此反应时间$t$应等于在理想管式反应器中的停留时间$\tau$,即$\tau = 2.5min$。
- 已知处理量$F_{A0}=0.684kmol/min$,$C_{A0}=4kmol/m^3$,则进料体积流量$V_0=\frac{F_{A0}}{C_{A0}}=\frac{0.684}{4}m^3/min = 0.171m^3/min$。
- 管式反应器的体积$V=\tau V_0=2.5\times0.171m^3 = 0.4275m^3\approx0.428m^3$。
- 计算管式反应器的长度$L$
- 已知管内径$D = 125mm = 0.125m$,根据$V=\frac{\pi}{4}D^2L$,可得$L=\frac{V}{\frac{\pi}{4}D^2}$。
- 代入$V = 0.428m^3$,$D = 0.125m$可得:
$L=\frac{0.428}{\frac{\pi}{4}\times(0.125)^2}m\approx35m$