题目
化合物X由三种元素组成,某学习小组按如图流程进行实验:白色固体-|||-H-|||-白色固体 无色溶液 HNO3 1.435g-|||-A G 足量-|||-X Na2CO 0.500g 浅黄色固体 氨水 无色溶液-|||-足量 足量 I-|||-195g 无色溶液 HI 棕黄色溶液 多次萃取 水溶液 AgNO 黄色固体-|||-B 足量 D 足量 Agl-|||-无色溶液已知:白色固体A用0.0250molHCl溶解后,多余的酸用0.0150molNaOH恰好中和。请回答:(1)X的组成元素是 ____ ,X的化学式是 ____ 。(2)写出B→C溶液呈棕黄色所发生的化学反应方程式 ____ 。(3)写出生成白色固体H的离子方程式 ____ 。(4)设计实验检验溶液Ⅰ中的阳离子 ____ 。
化合物X由三种元素组成,某学习小组按如图流程进行实验:
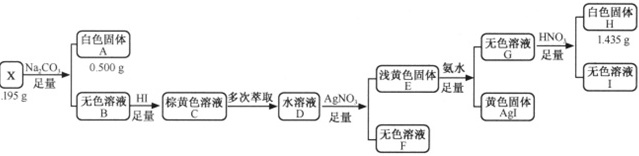
已知:白色固体A用0.0250molHCl溶解后,多余的酸用0.0150molNaOH恰好中和。
请回答:
(1)X的组成元素是 ____ ,X的化学式是 ____ 。
(2)写出B→C溶液呈棕黄色所发生的化学反应方程式 ____ 。
(3)写出生成白色固体H的离子方程式 ____ 。
(4)设计实验检验溶液Ⅰ中的阳离子 ____ 。

已知:白色固体A用0.0250molHCl溶解后,多余的酸用0.0150molNaOH恰好中和。
请回答:
(1)X的组成元素是 ____ ,X的化学式是 ____ 。
(2)写出B→C溶液呈棕黄色所发生的化学反应方程式 ____ 。
(3)写出生成白色固体H的离子方程式 ____ 。
(4)设计实验检验溶液Ⅰ中的阳离子 ____ 。
题目解答
答案
解:(1)通过以上分析知,X的组成元素是Ca、Cl、O,X的化学式是Ca(ClO4)2,
故答案为:Ca、Cl、O;Ca(ClO4)2;
(2)B中含有NaClO4,能氧化HI生成I2,同时生成NaCl、H2O,B→C溶液呈棕黄色所发生的化学反应方程式为8HI+NaClO4=4I2+NaCl+4H2O,
故答案为:8HI+NaClO4=4I2+NaCl+4H2O;
(3)G为银氨溶液,G和足量稀硝酸反应生成氯化银白色沉淀和氯化铵,生成白色固体H的离子方程式为[Ag(NH3)2]++Cl-+2H+=AgCl↓+2NH4+,
故答案为:[Ag(NH3)2]++Cl-+2H+=AgCl↓+2NH4+;
(4)I中含有NH4Cl、HNO3,酸遇蓝色石蕊试纸变红色,铵根离子和NaOH溶液反应生成NH3•H2O,加热NH3•H2O分解生成NH3,NH3能使湿润的红色石蕊试纸变蓝色,所以检验溶液Ⅰ中的阳离子方法为:用玻璃棒蘸取溶液I,点在蓝色石蕊试纸上,呈红色说明溶液中有H+;取溶液于试管中,加入NaOH至碱性,加热,将湿润的红色石蕊试纸置于试管口,若试纸变蓝说明有NH4+,
故答案为:用玻璃棒蘸取溶液I,点在蓝色石蕊试纸上,呈红色说明溶液中有H+;取溶液于试管中,加入NaOH至碱性,加热,将湿润的红色石蕊试纸置于试管口,若试纸变蓝说明有NH4+。
故答案为:Ca、Cl、O;Ca(ClO4)2;
(2)B中含有NaClO4,能氧化HI生成I2,同时生成NaCl、H2O,B→C溶液呈棕黄色所发生的化学反应方程式为8HI+NaClO4=4I2+NaCl+4H2O,
故答案为:8HI+NaClO4=4I2+NaCl+4H2O;
(3)G为银氨溶液,G和足量稀硝酸反应生成氯化银白色沉淀和氯化铵,生成白色固体H的离子方程式为[Ag(NH3)2]++Cl-+2H+=AgCl↓+2NH4+,
故答案为:[Ag(NH3)2]++Cl-+2H+=AgCl↓+2NH4+;
(4)I中含有NH4Cl、HNO3,酸遇蓝色石蕊试纸变红色,铵根离子和NaOH溶液反应生成NH3•H2O,加热NH3•H2O分解生成NH3,NH3能使湿润的红色石蕊试纸变蓝色,所以检验溶液Ⅰ中的阳离子方法为:用玻璃棒蘸取溶液I,点在蓝色石蕊试纸上,呈红色说明溶液中有H+;取溶液于试管中,加入NaOH至碱性,加热,将湿润的红色石蕊试纸置于试管口,若试纸变蓝说明有NH4+,
故答案为:用玻璃棒蘸取溶液I,点在蓝色石蕊试纸上,呈红色说明溶液中有H+;取溶液于试管中,加入NaOH至碱性,加热,将湿润的红色石蕊试纸置于试管口,若试纸变蓝说明有NH4+。
解析
步骤 1:确定X的组成元素
根据题意,X由三种元素组成,且通过实验流程可以推断出X的组成元素。从实验流程中,我们可以看到X与Na2CO3反应生成白色固体A,A与HCl反应生成无色溶液,无色溶液与氨水反应生成浅黄色固体,浅黄色固体与HI反应生成棕黄色溶液,棕黄色溶液与AgNO3反应生成黄色固体B。根据这些反应,可以推断出X的组成元素是Ca、Cl、O。
步骤 2:确定X的化学式
根据步骤1的推断,X的组成元素是Ca、Cl、O。根据实验流程,X与Na2CO3反应生成白色固体A,A与HCl反应生成无色溶液,无色溶液与氨水反应生成浅黄色固体,浅黄色固体与HI反应生成棕黄色溶液,棕黄色溶液与AgNO3反应生成黄色固体B。根据这些反应,可以推断出X的化学式是Ca(ClO4)2。
步骤 3:写出B→C溶液呈棕黄色所发生的化学反应方程式
根据实验流程,B与HI反应生成棕黄色溶液。根据化学反应原理,B中的NaClO4能氧化HI生成I2,同时生成NaCl、H2O。因此,B→C溶液呈棕黄色所发生的化学反应方程式为8HI+NaClO4=4I2+NaCl+4H2O。
步骤 4:写出生成白色固体H的离子方程式
根据实验流程,G为银氨溶液,G和足量稀硝酸反应生成氯化银白色沉淀和氯化铵。因此,生成白色固体H的离子方程式为[Ag(NH3)2]+ + Cl- + 2H+ = AgCl↓ + 2NH4+。
步骤 5:设计实验检验溶液Ⅰ中的阳离子
根据实验流程,I中含有NH4Cl、HNO3。酸遇蓝色石蕊试纸变红色,铵根离子和NaOH溶液反应生成NH3•H2O,加热NH3•H2O分解生成NH3,NH3能使湿润的红色石蕊试纸变蓝色。因此,检验溶液Ⅰ中的阳离子方法为:用玻璃棒蘸取溶液I,点在蓝色石蕊试纸上,呈红色说明溶液中有H+;取溶液于试管中,加入NaOH至碱性,加热,将湿润的红色石蕊试纸置于试管口,若试纸变蓝说明有NH4+。
根据题意,X由三种元素组成,且通过实验流程可以推断出X的组成元素。从实验流程中,我们可以看到X与Na2CO3反应生成白色固体A,A与HCl反应生成无色溶液,无色溶液与氨水反应生成浅黄色固体,浅黄色固体与HI反应生成棕黄色溶液,棕黄色溶液与AgNO3反应生成黄色固体B。根据这些反应,可以推断出X的组成元素是Ca、Cl、O。
步骤 2:确定X的化学式
根据步骤1的推断,X的组成元素是Ca、Cl、O。根据实验流程,X与Na2CO3反应生成白色固体A,A与HCl反应生成无色溶液,无色溶液与氨水反应生成浅黄色固体,浅黄色固体与HI反应生成棕黄色溶液,棕黄色溶液与AgNO3反应生成黄色固体B。根据这些反应,可以推断出X的化学式是Ca(ClO4)2。
步骤 3:写出B→C溶液呈棕黄色所发生的化学反应方程式
根据实验流程,B与HI反应生成棕黄色溶液。根据化学反应原理,B中的NaClO4能氧化HI生成I2,同时生成NaCl、H2O。因此,B→C溶液呈棕黄色所发生的化学反应方程式为8HI+NaClO4=4I2+NaCl+4H2O。
步骤 4:写出生成白色固体H的离子方程式
根据实验流程,G为银氨溶液,G和足量稀硝酸反应生成氯化银白色沉淀和氯化铵。因此,生成白色固体H的离子方程式为[Ag(NH3)2]+ + Cl- + 2H+ = AgCl↓ + 2NH4+。
步骤 5:设计实验检验溶液Ⅰ中的阳离子
根据实验流程,I中含有NH4Cl、HNO3。酸遇蓝色石蕊试纸变红色,铵根离子和NaOH溶液反应生成NH3•H2O,加热NH3•H2O分解生成NH3,NH3能使湿润的红色石蕊试纸变蓝色。因此,检验溶液Ⅰ中的阳离子方法为:用玻璃棒蘸取溶液I,点在蓝色石蕊试纸上,呈红色说明溶液中有H+;取溶液于试管中,加入NaOH至碱性,加热,将湿润的红色石蕊试纸置于试管口,若试纸变蓝说明有NH4+。