题目
写出下列电池的半电池反应及电池反应,计算电池的电动势,并标明电极的正负。(1) Zn∣ZnSO4(0.100mol/L)‖AgNO3(0.010mol/L)∣Ag(varphi )_({Zn)^2+}ZZn=-0.762V, . (varphi )_({A)_(A)'}^+,Ag=+0.80V(2) Pt,H2(20265Pa)∣HCl(0.100mol/L)‖HCl(0.100mol/L)∣Cl2(50663Pa),Pt(varphi )_({Zn)^2+}ZZn=-0.762V, . (varphi )_({A)_(A)'}^+,Ag=+0.80V, (varphi )_({Zn)^2+}ZZn=-0.762V, . (varphi )_({A)_(A)'}^+,Ag=+0.80V(3) Pb∣PbSO4(固),K2SO4(0.200mol/L)‖Pb(NO3)2(0.100mol/L)∣Pb(varphi )_({Zn)^2+}ZZn=-0.762V, . (varphi )_({A)_(A)'}^+,Ag=+0.80VKsp(PbSO4)=2.0x10-8(4) Zn∣(varphi )_({Zn)^2+}ZZn=-0.762V, . (varphi )_({A)_(A)'}^+,Ag=+0.80VO2(0.010mol/L),NaOH(0.500mol/L)‖HgO(固),NaOH(0.500mol/L)∣Hg(varphi )_({Zn)^2+}ZZn=-0.762V, . (varphi )_({A)_(A)'}^+,Ag=+0.80V
写出下列电池的半电池反应及电池反应,计算电池的电动势,并标明电极的正负。
(1) Zn∣ZnSO4(0.100mol/L)‖AgNO3(0.010mol/L)∣Ag
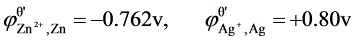
(2) Pt,H2(20265Pa)∣HCl(0.100mol/L)‖HCl(0.100mol/L)∣Cl2(50663Pa),Pt
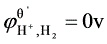 ,
, 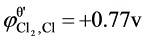
(3) Pb∣PbSO4(固),K2SO4(0.200mol/L)‖Pb(NO3)2(0.100mol/L)∣Pb
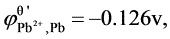 Ksp(PbSO4)=2.0x10-8
Ksp(PbSO4)=2.0x10-8(4) Zn∣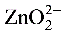 O2(0.010mol/L),NaOH(0.500mol/L)‖
O2(0.010mol/L),NaOH(0.500mol/L)‖
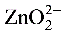 O2(0.010mol/L),NaOH(0.500mol/L)‖
O2(0.010mol/L),NaOH(0.500mol/L)‖HgO(固),NaOH(0.500mol/L)∣Hg

题目解答
答案
解:(1)半电池反应:ZnZn+2 + 2e, Ag+1 + eAg,
电池反应: Zn + 2Ag+1 = 2Ag + Zn+2
∵ 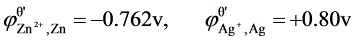
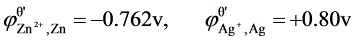
φ右=0.80 +(00591/1)lg0.01 =0.682
φ左=-0.762 +(00591/2)lg0.1 =-0.7916
∴电池的电动势E =φ右-φ左 =0.682-(-0.7916)=1.4736v
又 ∵ E>0 ∴ Ag为正极,Zn为负极。
解析
步骤 1:确定半电池反应
对于电池 Zn|ZnSO4(0.100mol/L)‖AgNO3(0.010mol/L)|Ag,半电池反应如下:
- 左侧半电池:Zn → Zn2+ + 2e- (氧化反应)
- 右侧半电池:Ag+ + e- → Ag (还原反应)
步骤 2:确定电池反应
将两个半电池反应合并,得到电池反应:
Zn + 2Ag+ → 2Ag + Zn2+
步骤 3:计算电池的电动势
根据能斯特方程,计算电池的电动势:
- 左侧半电池的电极电势:${\varphi }_{Zn^{2+}/Zn} = -0.762V + \frac{0.0591}{2} \log \frac{1}{0.100} = -0.762V + 0.02955V = -0.73245V$
- 右侧半电池的电极电势:${\varphi }_{Ag^{+}/Ag} = 0.80V + \frac{0.0591}{1} \log \frac{1}{0.010} = 0.80V + 0.1182V = 0.9182V$
- 电池的电动势:E = ${\varphi }_{Ag^{+}/Ag} - {\varphi }_{Zn^{2+}/Zn} = 0.9182V - (-0.73245V) = 1.65065V$
步骤 4:确定电极的正负
由于电池的电动势为正,所以右侧的Ag为正极,左侧的Zn为负极。
对于电池 Zn|ZnSO4(0.100mol/L)‖AgNO3(0.010mol/L)|Ag,半电池反应如下:
- 左侧半电池:Zn → Zn2+ + 2e- (氧化反应)
- 右侧半电池:Ag+ + e- → Ag (还原反应)
步骤 2:确定电池反应
将两个半电池反应合并,得到电池反应:
Zn + 2Ag+ → 2Ag + Zn2+
步骤 3:计算电池的电动势
根据能斯特方程,计算电池的电动势:
- 左侧半电池的电极电势:${\varphi }_{Zn^{2+}/Zn} = -0.762V + \frac{0.0591}{2} \log \frac{1}{0.100} = -0.762V + 0.02955V = -0.73245V$
- 右侧半电池的电极电势:${\varphi }_{Ag^{+}/Ag} = 0.80V + \frac{0.0591}{1} \log \frac{1}{0.010} = 0.80V + 0.1182V = 0.9182V$
- 电池的电动势:E = ${\varphi }_{Ag^{+}/Ag} - {\varphi }_{Zn^{2+}/Zn} = 0.9182V - (-0.73245V) = 1.65065V$
步骤 4:确定电极的正负
由于电池的电动势为正,所以右侧的Ag为正极,左侧的Zn为负极。