根据dG=-SdT+Vdp+ ∠βB/dnB,可知任意化学反应的dG=-SdT+Vdp+ ∠βB/dnB______________A. 放热反应 B. 吸热反应 C. 无法判断 D. 体积缩小的反应 E. K时N2O4(g)=2NO2(g)的Kø =0.142,当p(N2O4)=101.325kPa,p(NO2)=10.133kPa 时,判断反应的方向为( )。 F. Jp<Kø,自发进行 G. Jp > Kø,非自发进行 Jp = Kø,平衡 Jp < Kø,非自发进行 ( ) 197. 某反应的的速率常数k=4.62×10-2min-1,又初始浓度为0.1mol·dm-3,则该反应的半衰期为t1/2( )。 1/(6.93×10-2×0.12) 15 30 1(4.62×102×0.1) ( ) 198. 对于一个化学反应来说,下列说法中正确的是( )。 △S≠越负,反应速率越快 △H≠越负,反应速率越快 活化能越大,反应速率越快 活化能越小,反应速率越快 ( ) 199. 催化剂加快反应速率,是由于它能使( )。 指前因子增大 几率因子增大 活化分子数增加 碰撞频率增加 ( )200. 反应本性、温度、反应途径、浓度与活化能关系正确的是( )。 反应途径与活化能无关 反应物浓度与活化能有关 反应温度与活化能无关 反应本性与活化能有关 ( )201. 不饱和溶液中溶质的化学势与纯溶质的化学势*的关系为( ) >* =* C <* D 无法确定 2H5OH(l)+3O2(g) →2CO2(g)+3H2O(g)的反应焓为ΔrHmθ, ΔCp>0, 下列说法中正确的是( ) ΔrHmθ是C2H5OH(l)的标准摩尔燃烧焓 ΔrHmθ〈0 ΔrHmθ=ΔrUmθ ΔrHmθ不随温度变化而变化 (s),H2O(g),CO(g),CO2(g),H2(g),它们之间存在三个平衡: (s)+H2O(g) = CO(g)+ H2(g);CO2(g)+H2(g) = CO(g)+ H2O(g);C(s)+CO2(g) = CO(g)则该系统的独立组分数C为( ) 3 2 1 4 K3[Fe(CN)6]水溶液,其质量摩尔浓度为b,离子平均活度系数为dG=-SdT+Vdp+ ∠βB/dnB,则此溶液的离子平均活度adG=-SdT+Vdp+ ∠βB/dnB等于( ) dG=-SdT+Vdp+ ∠βB/dnB dG=-SdT+Vdp+ ∠βB/dnB dG=-SdT+Vdp+ ∠βB/dnB dG=-SdT+Vdp+ ∠βB/dnB K时,KNO3水溶液的浓度由1mol·dm-3增大到2 mol·dm-3,其摩尔电导率Λm将( ) 增大 减小 不变 不确定 K时,下列两电极反应的标准电极电势为: e3+ + 3e-→ Fe Eθ(Fe3+/Fe)=-0.036V e2+ + 2e-→ Fe Eθ(Fe2+/Fe)=-0.439V e3+ + e-→ Fe2+ 的Eθ(Pt/Fe3+, Fe2+)等于 ( ) 0.184V 0.352V -0.184V 0.770V ( ) 207. 对于水平液面,其值为零的物理量是( ) 表面自由能 表面张力 附加压力 比表面能 ( ) 208. 下列各性质中不属于溶胶动力学性质的是( ) 布郎运动 扩散 电泳 沉降平衡 ( ) 209. 凡溶胶达到等电状态,说明胶粒 ( ) 带电,易聚沉 不带电,很易聚沉 带电,不易聚沉 不带电,不易聚沉 ( )210. 下列函数中为强度性质的是( ) S (G/p)T (U/V)T CV ( )211. 某反应的速率常数为3.93×10-2s-1,那这个反应的t1/2为 ( ) 30.0 s 17.6 s C.8.0 s D.14.5 s (s)+H2O(g)→H2(g)+CO(g) 在1000K时,Kø =2.472,ΔrHmø=1.36×105J·mol-1,ΔCp=0,则1200K时Kø的值( ) 10.94 3.758 1.631 37.58 ( )213. 如右图所示,当水处在三相点平衡时,若系统发生绝热膨胀,水的相态将如何变化? dG=-SdT+Vdp+ ∠βB/dnB ( ) 气相、固相消失,全部变成液态 气相、液相消失,全部变成固态 液相消失,固相、气相共存 固相消失,液相、气相共存 ( )214. 下列公式中需要“不做非体积功”的条件的是( )。 H = U + (pV) S = (δQr/T) ΔS(T→0 K)= 0 GT,p 0 作判据 ( )215. 有两个反应,其速率方程均满足r=kc n,已知k1>k2,且c1=c2=2mol·dm-3时,r1<r2,则两个反应的级数 ( ) 。 n1>n2 n1=n2 n1<n2 前三者均有可能 ( )216. 某化学反应其反应物消耗8/7所需的时间是它消耗掉4/3所需的时间的1.5倍,则反应的级数为( )。 零级反应 一级反应 二级反应 三级反应 KI存在的AgI溶胶,哪一种电解质的聚沉能力最强( ) FeCldG=-SdT+Vdp+ ∠βB/dnB MgSO2+ KdG=-SdT+Vdp+ ∠βB/dnB [Fe(CN)dG=-SdT+Vdp+ ∠βB/dnB] MgCldG=-SdT+Vdp+ ∠βB/dnB ( )218. 已知乙醇和水形成的最低共沸混合物中含水4.43%。某酒厂酿制的白酒含乙醇35%,欲用分馏法分离提纯,最终可得到( ) 纯水和纯乙醇 B.纯乙醇与共沸物 C.纯水与共沸物 D.纯乙醇 发生吸附,若CdG=-SdT+Vdp+ ∠βB/dnB(表面浓度)< dG=-SdT+Vdp+ ∠βB/dnBdG=-SdT+Vdp+ ∠βB/dnB(本体浓度),则( ) 称为负吸附,溶液表面张力σ增加 称为正吸附,溶液表面张力σ增加 称为负吸附,溶液表面张力σ下降 称为正吸附,溶液表面张力σ下降 K时反应Zn+Fe-2=Zn-1+Fe的E-3为0.323V,则其平衡常数为 2.89×101/2 8.34×10-2 C. 5.53×102 D. 2.35×102 uSO4水溶液置于绝热箱中,插入两个铜电 极,以蓄电池为电源进行电解,可以看作封闭体系的是( )。 绝热箱中所有物质 两个铜电极 蓄电池和铜电极 CuSO水溶液 V输出电压放电后,用2.2 V电压充电使其回复原状,则总的过程热力学量变化( )。 Q < 0,W > 0,∆S > 0,∆G < 0 Q < 0,W < 0,∆S < 0,∆G < 0 Q > 0,W > 0,∆S = 0,∆G = 0 Q < 0,W > 0,∆S = 0,∆G = 0 ( ) 223. 在一定速度下发生变化的孤立体系,其总熵的变化( )。 不变 可能增大或减小 总是增大 总是减小 → 和A→ 均为理想气体变化过程,若B、C在同一条绝热线上,那么∆U与∆U的关系是: ∆U > ∆U ∆U < ∆U ∆U = ∆U 无法比较两者大小 S为负值的是( )。 液态溴蒸发成气态溴 SnO(s) + 2H(g) = Sn(s) + 2HO(l) 电解水生成H和O 公路上撤盐使冰融化 (s) = D(g) + G(g) 的∆G(J·mol) = -4500 + 11(T/K), 要防止反应发生,温度必须( )。 高于409K 低于136K 高于136K而低于409K 低409K 。 ( ) 227. 下列叙述中不正确的是( )。 标准平衡常数仅是温度的函数 催化剂不能改变平衡常数的大小 平衡常数发生变化,化学平衡必定发生移动,达到新的平衡 化学平衡发生新的移动,平衡常数必发生变化 =2的体系是( )。 298K时,HO(l)与HO(g)共存 S(s)、S(l)、S(g)共存 一定量的PCl(g) 分解平衡时:PCl(g) = PCl(g) + Cl(g) CHOH(l) 与HO(l) 的混合物 两杯稀盐水溶液,盐的浓度分别为c和 (c > c),放置足够长的时间后( )。 A杯盐的浓度降低,B杯盐的浓度增加 A杯液体量减少,B杯液体量增加 A杯盐的浓度增加,B杯盐的浓度降低 A、B两杯中盐的浓度会同时增大 H(g) + S(s) = HS(s) ① K ; (s) + O(g) = SO(g) ② K 。则反应 H(g) + SO(g) = O(g) + HS(g) 的平衡常数为( ) K + K K - K K·K K/K ( ) 231. 某电池的电池反应可写成: H (g)+ O (g) HO(l) H (g)+ O (g) 2HO(l) ,E和K,K表示,则 ( ) E=E K=K E≠E K=K E=E K≠K =E K≠K D.E≠E K≠K ( ) 232在下列体系中自由度f = 2的体系是( ) 298K时,HO(l)、HO(g) 平衡 S(s)、S(l)、S(g) 平衡 CHOH(l) 与HO(l) 的混合物 一定量的PCl(g) 分解平衡时:PCl(g) = PCl(g) + Cl(g) Q = -200 J 时,其焓变ΔH为( ) ΔH = -200 J ; ΔH < -200 J ; ΔH = 0 ; ΔH > -200 J 。 K时进行的速度较慢,在305K时更慢,该吸附过程主要是( ) 物理吸附 化学吸附 不能确定 物理吸附与化学吸附同时发生 ( ) 235毛笔蘸上水,笔毛就会粘在一起,这是因为 ( )。 笔毛上的水在空气中有自动收缩减小表面的趋势 笔毛被润湿 水是表面活性物质 水具有粘度 ( ) 236. 某温度时,对十二烷基苯磺酸钠的σ~c曲线如图所示, 图中说明烃基为直链时比带有支链时表面活性剂的( ) 效率高,有效值小 效率低,有效值大 效率高,有效值大 效率低,有效值小 ( ) 237. 在描述一级反应的下列说法中,不正确的是( )。 ㏑c对时间t作图得一直线 半衰期与反应物起始浓度成反比 同一反应消耗反应物的百分数相同时,所需时间相等 速率常数的单位为(时间)-1 ( ) 238. 对ζ电势的阐述,正确的是: ζ电势与溶剂化层中离子浓度有关 ζ电势在无外电场作用下也可表示出来 |ζ| 电势越大,溶胶越不稳定 |ζ| 电势越大,扩散层中反号离子越少 ( ) 239.下面对于催化剂的特征描述,不正确的是( )。 酶只能缩短反应达到平衡的时间而不能改变平衡态 酶在反应前后其化学性质和物理性质皆不变 酶不能改变平衡常数 酶不能实现热力学上不可能进行的反应 ( )240. 某反应的的速率常数k=4.62×10min,又初始浓度为0.1mol·dm,则该反应的半衰期为t( ) 1/(6.93×10×0.1) 15 30 1(4.62×10×0.1)
根据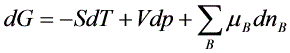 ,可知任意化学反应的
,可知任意化学反应的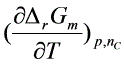 ______________
______________
B. 吸热反应
C. 无法判断
D. 体积缩小的反应
E. K时N2O4(g)=2NO2(g)的Kø =0.142,当p(N2O4)=101.325kPa,p(NO2)=10.133kPa 时,判断反应的方向为( )。
F. Jp<Kø,自发进行
G. Jp > Kø,非自发进行
Jp = Kø,平衡
Jp < Kø,非自发进行
( ) 197. 某反应的的速率常数k=4.62×10-2min-1,又初始浓度为0.1mol·dm-3,则该反应的半衰期为t1/2( )。
1/(6.93×10-2×0.12)
15
30
1(4.62×102×0.1)
( ) 198. 对于一个化学反应来说,下列说法中正确的是( )。
△S≠越负,反应速率越快
△H≠越负,反应速率越快
活化能越大,反应速率越快
活化能越小,反应速率越快
( ) 199. 催化剂加快反应速率,是由于它能使( )。
指前因子增大
几率因子增大
活化分子数增加
碰撞频率增加
( )200. 反应本性、温度、反应途径、浓度与活化能关系正确的是( )。
反应途径与活化能无关
反应物浓度与活化能有关
反应温度与活化能无关
反应本性与活化能有关
( )201. 不饱和溶液中溶质的化学势与纯溶质的化学势*的关系为( )
>*
=* C <* D 无法确定
2H5OH(l)+3O2(g) →2CO2(g)+3H2O(g)的反应焓为ΔrHmθ, ΔCp>0, 下列说法中正确的是( )
ΔrHmθ是C2H5OH(l)的标准摩尔燃烧焓
ΔrHmθ〈0
ΔrHmθ=ΔrUmθ
ΔrHmθ不随温度变化而变化
(s),H2O(g),CO(g),CO2(g),H2(g),它们之间存在三个平衡:
(s)+H2O(g) = CO(g)+ H2(g);CO2(g)+H2(g) = CO(g)+ H2O(g);C(s)+CO2(g) = CO(g)则该系统的独立组分数C为( )
3
2
1
4
K3[Fe(CN)6]水溶液,其质量摩尔浓度为b,离子平均活度系数为
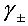 ,则此溶液的离子平均活度a
,则此溶液的离子平均活度a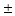 等于( )
等于( )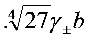
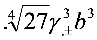
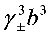
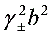
K时,KNO3水溶液的浓度由1mol·dm-3增大到2 mol·dm-3,其摩尔电导率Λm将( )
增大
减小
不变
不确定
K时,下列两电极反应的标准电极电势为:
e3+ + 3e-→ Fe Eθ(Fe3+/Fe)=-0.036V
e2+ + 2e-→ Fe Eθ(Fe2+/Fe)=-0.439V
e3+ + e-→ Fe2+ 的Eθ(Pt/Fe3+, Fe2+)等于 ( )
0.184V
0.352V
-0.184V
0.770V
( ) 207. 对于水平液面,其值为零的物理量是( )
表面自由能
表面张力
附加压力
比表面能
( ) 208. 下列各性质中不属于溶胶动力学性质的是( )
布郎运动
扩散
电泳
沉降平衡
( ) 209. 凡溶胶达到等电状态,说明胶粒 ( )
带电,易聚沉
不带电,很易聚沉
带电,不易聚沉
不带电,不易聚沉
( )210. 下列函数中为强度性质的是( )
S
(G/p)T
(U/V)T
CV
( )211. 某反应的速率常数为3.93×10-2s-1,那这个反应的t1/2为 ( )
30.0 s
17.6 s C.8.0 s D.14.5 s
(s)+H2O(g)→H2(g)+CO(g) 在1000K时,Kø =2.472,ΔrHmø=1.36×105J·mol-1,ΔCp=0,则1200K时Kø的值( )
10.94
3.758
1.631
37.58
( )213. 如右图所示,当水处在三相点平衡时,若系统发生绝热膨胀,水的相态将如何变化?
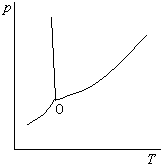 ( )
( )气相、固相消失,全部变成液态
气相、液相消失,全部变成固态
液相消失,固相、气相共存
固相消失,液相、气相共存
( )214. 下列公式中需要“不做非体积功”的条件的是( )。
H = U + (pV)
S = (δQr/T)
ΔS(T→0 K)= 0
GT,p 0 作判据
( )215. 有两个反应,其速率方程均满足r=kc n,已知k1>k2,且c1=c2=2mol·dm-3时,r1<r2,则两个反应的级数 ( ) 。
n1>n2
n1=n2
n1<n2
前三者均有可能
( )216. 某化学反应其反应物消耗8/7所需的时间是它消耗掉4/3所需的时间的1.5倍,则反应的级数为( )。
零级反应
一级反应
二级反应
三级反应
KI存在的AgI溶胶,哪一种电解质的聚沉能力最强( )
FeCl
MgSO2+
K
 [Fe(CN)
[Fe(CN)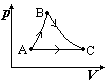 ]
]MgCl
( )218. 已知乙醇和水形成的最低共沸混合物中含水4.43%。某酒厂酿制的白酒含乙醇35%,欲用分馏法分离提纯,最终可得到( )
纯水和纯乙醇 B.纯乙醇与共沸物 C.纯水与共沸物 D.纯乙醇
发生吸附,若C
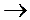 (表面浓度)<
(表面浓度)<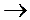
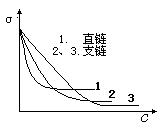 (本体浓度),则( )
(本体浓度),则( )称为负吸附,溶液表面张力σ增加
称为正吸附,溶液表面张力σ增加
称为负吸附,溶液表面张力σ下降
称为正吸附,溶液表面张力σ下降
K时反应Zn+Fe-2=Zn-1+Fe的E-3为0.323V,则其平衡常数为
2.89×101/2
8.34×10-2 C. 5.53×102 D. 2.35×102
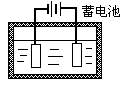
uSO4水溶液置于绝热箱中,插入两个铜电
极,以蓄电池为电源进行电解,可以看作封闭体系的是( )。
绝热箱中所有物质
两个铜电极
蓄电池和铜电极
CuSO水溶液
V输出电压放电后,用2.2 V电压充电使其回复原状,则总的过程热力学量变化( )。
Q < 0,W > 0,∆S > 0,∆G < 0
Q < 0,W < 0,∆S < 0,∆G < 0
Q > 0,W > 0,∆S = 0,∆G = 0
Q < 0,W > 0,∆S = 0,∆G = 0
( ) 223. 在一定速度下发生变化的孤立体系,其总熵的变化( )。
不变
可能增大或减小
总是增大
总是减小
→
和A→
均为理想气体变化过程,若B、C在同一条绝热线上,那么∆U与∆U的关系是:
∆U > ∆U
∆U < ∆U
∆U = ∆U
无法比较两者大小
S为负值的是( )。
液态溴蒸发成气态溴
SnO(s) + 2H(g) = Sn(s) + 2HO(l)
电解水生成H和O
公路上撤盐使冰融化
(s) = D(g) + G(g) 的∆G(J·mol) = -4500 + 11(T/K),
要防止反应发生,温度必须( )。
高于409K
低于136K
高于136K而低于409K
低409K 。
( ) 227. 下列叙述中不正确的是( )。
标准平衡常数仅是温度的函数
催化剂不能改变平衡常数的大小
平衡常数发生变化,化学平衡必定发生移动,达到新的平衡
化学平衡发生新的移动,平衡常数必发生变化
=2的体系是( )。
298K时,HO(l)与HO(g)共存
S(s)、S(l)、S(g)共存
一定量的PCl(g) 分解平衡时:PCl(g) = PCl(g) + Cl(g)
CHOH(l) 与HO(l) 的混合物
两杯稀盐水溶液,盐的浓度分别为c和
(c > c),放置足够长的时间后( )。
A杯盐的浓度降低,B杯盐的浓度增加
A杯液体量减少,B杯液体量增加
A杯盐的浓度增加,B杯盐的浓度降低
A、B两杯中盐的浓度会同时增大
H(g) + S(s) = HS(s) ① K ;
(s) + O(g) = SO(g) ② K 。则反应 H(g) + SO(g) = O(g) + HS(g)
的平衡常数为( )
K + K
K - K
K·K
K/K
( ) 231. 某电池的电池反应可写成:
H (g)+ O (g) HO(l)
H (g)+ O (g) 2HO(l)
,E和K,K表示,则 ( )
E=E K=K
E≠E K=K
E=E K≠K
=E K≠K D.E≠E K≠K
( ) 232在下列体系中自由度f = 2的体系是( )
298K时,HO(l)、HO(g) 平衡
S(s)、S(l)、S(g) 平衡
CHOH(l) 与HO(l) 的混合物
一定量的PCl(g) 分解平衡时:PCl(g) = PCl(g) + Cl(g)
Q = -200 J 时,其焓变ΔH为( )
ΔH = -200 J ;
ΔH < -200 J ;
ΔH = 0 ;
ΔH > -200 J 。
K时进行的速度较慢,在305K时更慢,该吸附过程主要是( )
物理吸附
化学吸附
不能确定
物理吸附与化学吸附同时发生
( ) 235毛笔蘸上水,笔毛就会粘在一起,这是因为 ( )。
笔毛上的水在空气中有自动收缩减小表面的趋势
笔毛被润湿
水是表面活性物质
水具有粘度
( ) 236. 某温度时,对十二烷基苯磺酸钠的σ~c曲线如图所示,
图中说明烃基为直链时比带有支链时表面活性剂的( )
效率高,有效值小
效率低,有效值大
效率高,有效值大
效率低,有效值小
( ) 237. 在描述一级反应的下列说法中,不正确的是( )。
㏑c对时间t作图得一直线
半衰期与反应物起始浓度成反比
同一反应消耗反应物的百分数相同时,所需时间相等
速率常数的单位为(时间)-1
( ) 238. 对ζ电势的阐述,正确的是:
ζ电势与溶剂化层中离子浓度有关
ζ电势在无外电场作用下也可表示出来
|ζ| 电势越大,溶胶越不稳定
|ζ| 电势越大,扩散层中反号离子越少
( ) 239.下面对于催化剂的特征描述,不正确的是( )。
酶只能缩短反应达到平衡的时间而不能改变平衡态
酶在反应前后其化学性质和物理性质皆不变
酶不能改变平衡常数
酶不能实现热力学上不可能进行的反应
( )240. 某反应的的速率常数k=4.62×10min,又初始浓度为0.1mol·dm,则该反应的半衰期为t( )
1/(6.93×10×0.1)
15
30
1(4.62×10×0.1)
题目解答
答案
( )200. 反应本性、温度、反应途径、浓度与活化能关系正确的是 ( ) 。 A. 反应途径与活化能无关 B. 反应物浓度与活化能有关 C. 反应温度与活化能无关 D. 反应本性与活化能有关 20 ( ) 20 2. 在标准状态下,反应 C 2 H 5 OH ( l ) +3O 2 (g) → 2CO 2 (g)+3H 2 O(g) 的反应焓为Δ r H m θ , Δ C p >0, 下列说法中正确的是( ) A. Δ r H m θ 是 C 2 H 5 OH ( l )的标准摩尔燃烧焓 B. Δ r H m θ 〈0 C. Δ r H m θ =Δ r U m θ D. Δ r H m θ 不随温度变化而变化 20 20 K 3 [Fe(CN) 6 ] 水溶液,其质量摩尔浓度为 b ,离子平均活度系数为 ,则此溶液 的离子平均活度 a 等于( ) A. B . C. D. 20 298K 时, KNO 3 水溶液的浓度由 1mol · dm -3 增大到 2 mol · dm -3 , 其摩尔电导率Λ m 将 ( ) A. 增大 B. 减小 C. 不变 D. 不确定 20 298K 时,下列两电极反应的标准电极电势为 : Fe 3+ + 3e - → Fe E θ (Fe 3+ /Fe)=-0.036V Fe 2+ + 2e - → Fe E θ (Fe 2+ /Fe)=-0.439V 则反应 Fe 3+ + e - → Fe 2+ 的 E θ (Pt/Fe 3+ , Fe 2+ ) 等于 ( ) A.0.184V B.0.352V C.-0.184V D.0.770V 20 对于水平液面,其值为零的物理量是 ( ) A. 表面自由能 B. 表面张力 C. 附加压力 D. 比表面能 20 下列各性质中不属于溶胶动力学性质的是 ( ) A . 布郎运动 B . 扩散 C . 电泳 D . 沉降平衡 20 凡溶胶达到等电状态,说明胶粒 ( ) A . 带电,易聚沉 B . 不带电,很易聚沉 C. 带电,不易聚沉 D. 不带电,不易聚沉 某反应的速率常数为 3.93 × 10 -2 s -1 ,那这个反应的 t 1/2 为 ( ) A. 30.0 s B. 17.6 s C. 8.0 s D. 14.5 s 已知反应 C(s)+H 2 O(g) → H 2 (g)+CO(g) 在 1000K 时, K ø =2.472 ,Δ r H m ø =1.36 × 10 5 J · mol -1 ,Δ C p =0 ,则 1200K 时 K ø 的值 ( ) A.10.94 B.3.758 C.1.631 D.37.58 13. 如右图所示,当水处在三相点平衡时,若系统发生绝热膨胀,水的相态将如何变化? ( ) A. 气相、固相消失,全部变成液态 B. 气相、液相消失,全部变成固态 C. 液相消失,固相、气相共存 D. 固相消失,液相、气相共存 下列公式中需要 “ 不做非体积功 ” 的条件的是 。 A. H = U + ( pV ) B. S = ( δ Q r / T ) C. Δ S ( T →0 K ) = 0 D. G T,p 0 作判据 有两个反应,其速率方程均满足 r = kc n ,已知 k 1 > k 2 ,且 c 1 = c 2 =2mol · dm -3 时, r 1 < r 2 ,则两个反应的级数 ( ) 。 A. n 1 > n 2 B. n 1 = n 2 C. n 1 < n 2 D. 前三者均有可能 ( ) 2 16. 某化学反应其反应物消耗 8/7 所需的时间是它消耗掉 4/3 所需的时间的 1.5 倍,则反应的级数为 ( )。 A. 零级反应 B. 一级反应 C. 二级反应 D. 三级反应 对于有过量 KI 存在的 AgI 溶胶,哪一种电解质的聚沉能力最强( ) A. FeCl B. MgSO 4 C. K [Fe ( CN ) ] D.MgCl 溶液表面层对溶质 B 发生吸附,若 C (表面浓度) < C (本体浓度),则( ) A. 称为负吸附,溶液表面张力σ增加 B. 称为正吸附,溶液表面张力σ增加 C. 称为负吸附,溶液表面张力σ下降 D. 称为正吸附,溶液表面张力σ下降 ( ) 2 20. 298K 时反应 Zn+Fe 2+ =Zn 2+ +Fe 的 E 0 为 0.323V ,则其平衡常数为 A. 2.89 × 10 5 B. 8.34 × 10 10 C. 5.53 × 10 4 D. 2.35 × 10 2 2 2 2 2 一个已充电的蓄电池以 1.8 V 输出电压放电后,用 2.2 V 电压充电使其回复原状,则总的过程热力学量变化 A Q < 0 , W > 0 , ∆ S > 0 , ∆ G < 0 B Q < 0 , W < 0 , ∆ S < 0 , ∆ G < 0 C Q > 0 , W > 0 , ∆ S = 0 , ∆ G = 0 D Q < 0 , W > 0 , ∆ S = 0 , ∆ G = 0 2 2 在一定速度下发生变化的孤立体系,其总熵的变化 A 不变 B 可能增大或减小 C 总是增大 D 总是减小 2 2 ( ) 2 2 5. 下列过程中 ∆ S 为负值的是 A 液态溴蒸发成气态溴 B SnO 2 (s) + 2H 2 (g) = Sn(s) + 2H 2 O(l) C 电解水生成 H 2 和 O 2 D 公路上撤盐使冰融化 2 2 设反应 A(s) = D(g) + G(g) 的 ∆ r G m (J · mol -1 ) = -4500 + 11( T /K) , 要防止反应发生,温度必须 A 高于 409K B 低于 136K C 高于 136K 而低于 409K D 低 409K 。 2 2 下列叙述中不正确的是 A 标准平衡常数仅是温度的函数 B 催化剂不能改变平衡常数的大小 C 平衡常数发生变化,化学平衡必定发生移动,达到新的平衡 D 化学平衡发生新的移动,平衡常数必发生变化 ( ) 2 2 8. 在下列体系中自由度 F =2 的体系是 A 298K 时, H 2 O(l) 与 H 2 O(g) 共存 B S(s) 、 S(l) 、 S(g) 共存 C 一定量的 PCl 5 (g) 分解平衡时: PCl 5 (g) = PCl 3 (g) + Cl 2 (g) D C 2 H 5 OH(l) 与 H 2 O(l) 的混合物 2 2 某电池的电池反应可写成 : ( 1 ) H 2 (g)+ O 2 (g) H 2 O(l) ( 2 ) 2H 2 (g)+ O 2 (g) 2H 2 O(l) 相应的电动势和化学反应平衡常数分别用 E 1 , E 2 和 K 1 , K 2 表示,则 ( ) A.E 1 =E 2 K 1 =K 2 B.E 1 ≠ E 2 K 1 =K 2 C.E 1 =E 2 K 1 ≠ K 2 D.E 1 ≠ E 2 K 1 ≠ K 2 ( ) 2 在下列体系中自由度 f = 2 的体系是 ( ) A.298K 时 , H 2 O(l) 、 H 2 O(g) 平衡 B. S(s) 、 S(l) 、 S(g) 平衡 C. C 2 H 5 OH(l) 与 H 2 O(l) 的混合物 D. 一定量的 PCl 5 (g) 分解平衡时: PCl 5 (g) = PCl 3 (g) + Cl 2 (g) ( ) 3. 某电池在标准状况下,放电过程中,当 Q r = -200 J 时,其焓变 Δ H 为 ( ) A. Δ H = -200 J ; B. Δ H < -200 J ; C. Δ H = 0 ; D. Δ H > -200 J 。 5 毛笔蘸上水,笔毛就会粘在一起,这是因为 ( ) 。 A . 笔毛上的水在空气中有自动收缩减小表面的趋势 B . 笔毛被润湿 C . 水是表面活性物质 D . 水具有粘度 7. 在描述一级反应的下列说法中,不正确的是( )。 A. ㏑ c 对时间 t 作图得一直线 B. 半衰期与反应物起始浓度成反比 C. 同一反应消耗反应物的百分数相同时,所需时间相等 D. 速率常数的单位为(时间) -1