题目
3.11 用 .1000molcdot (L)^-1NaOH 溶液滴定 .1000molcdot (L)^-1 甲酸溶液,化学计量点的 -|||-是多少?计算用酚酞作指示剂(pT为9.0)时的终点误差。

题目解答
答案
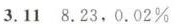
解析
步骤 1:计算化学计量点的pH值
在化学计量点,甲酸(HCOOH)与氢氧化钠(NaOH)完全反应,生成甲酸钠(HCOONa)和水(H2O)。甲酸钠在水中水解,产生OH-离子,导致溶液呈碱性。甲酸的Ka值为$1.8 \times 10^{-4}$,因此甲酸钠的Kb值为$10^{-14}/1.8 \times 10^{-4} = 5.56 \times 10^{-11}$。在化学计量点,甲酸钠的浓度为$0.0500mol\cdot {L}^{-1}$,因此可以计算OH-离子的浓度,进而计算pH值。
步骤 2:计算终点误差
终点误差是指滴定终点与化学计量点之间的差异。酚酞的pT值为9.0,意味着在pH为9.0时,酚酞指示剂的颜色变化最为明显。因此,终点误差可以通过计算pH为9.0时的OH-离子浓度与化学计量点时的OH-离子浓度之间的差异来确定。
步骤 3:计算终点误差的百分比
将步骤2中计算得到的终点误差除以化学计量点时的OH-离子浓度,然后乘以100%,得到终点误差的百分比。
在化学计量点,甲酸(HCOOH)与氢氧化钠(NaOH)完全反应,生成甲酸钠(HCOONa)和水(H2O)。甲酸钠在水中水解,产生OH-离子,导致溶液呈碱性。甲酸的Ka值为$1.8 \times 10^{-4}$,因此甲酸钠的Kb值为$10^{-14}/1.8 \times 10^{-4} = 5.56 \times 10^{-11}$。在化学计量点,甲酸钠的浓度为$0.0500mol\cdot {L}^{-1}$,因此可以计算OH-离子的浓度,进而计算pH值。
步骤 2:计算终点误差
终点误差是指滴定终点与化学计量点之间的差异。酚酞的pT值为9.0,意味着在pH为9.0时,酚酞指示剂的颜色变化最为明显。因此,终点误差可以通过计算pH为9.0时的OH-离子浓度与化学计量点时的OH-离子浓度之间的差异来确定。
步骤 3:计算终点误差的百分比
将步骤2中计算得到的终点误差除以化学计量点时的OH-离子浓度,然后乘以100%,得到终点误差的百分比。