题目
甲、乙、丙三种固体的溶解度曲线如图1所示,如图2是选用图1中某种固体进行实验时的情况。下列说法正确的是( )↑溶解度/g 甲-|||-80 向烧杯中加入-|||-60 NaOH固体-|||-乙-|||-40-|||-20 丙-|||-试管中固体 试管中固体-|||-0 t1 t2 t3 温度/℃ 未完全溶解 完全溶解-|||-图1 图2A. 图2试管中固体对应图1中的丙B. t2℃时,甲、乙两饱和溶液中溶质质量相等C. t3℃时,将40g甲加入到50g水中,所得溶液的溶质质量分数为80%D. 将等质量的甲、乙、丙饱和溶液从t2℃降温到t1℃,得到溶液的质量:丙>乙>甲
甲、乙、丙三种固体的溶解度曲线如图1所示,如图2是选用图1中某种固体进行实验时的情况。下列说法正确的是( )
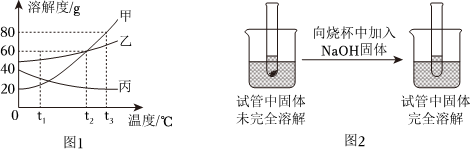

- A. 图2试管中固体对应图1中的丙
- B. t2℃时,甲、乙两饱和溶液中溶质质量相等
- C. t3℃时,将40g甲加入到50g水中,所得溶液的溶质质量分数为80%
- D. 将等质量的甲、乙、丙饱和溶液从t2℃降温到t1℃,得到溶液的质量:丙>乙>甲
题目解答
答案
解:A、氢氧化钠固体溶于水放热,使温度升高,试管内的原来剩余的固体完全溶解,说明该物质的溶解度随着温度的升高而增大,图2试管中固体对应的不可能是图1中的丙,故选项说法错误。
B、选项说法没有指明饱和溶液的质量,则t2℃时甲、乙两饱和溶液中溶质质量不一定相等,故选项说法错误。
C、t3℃时,甲的溶解度为80g,将40g甲加入到50g水中,最多能溶解40g,所得溶液的溶质质量分数为$\frac{40g}{40g+50g}$×100%≈44.4%,故选项说法错误。
D、将等质量的甲、乙、丙饱和溶液从t2℃降温到t1℃,甲、乙的溶解度减小,有晶体析出,t1℃时乙的溶解度大于甲,丙的溶解度增大,没有晶体析出,则得到溶液的质量:丙>乙>甲,故选项说法正确。
故选:D。
B、选项说法没有指明饱和溶液的质量,则t2℃时甲、乙两饱和溶液中溶质质量不一定相等,故选项说法错误。
C、t3℃时,甲的溶解度为80g,将40g甲加入到50g水中,最多能溶解40g,所得溶液的溶质质量分数为$\frac{40g}{40g+50g}$×100%≈44.4%,故选项说法错误。
D、将等质量的甲、乙、丙饱和溶液从t2℃降温到t1℃,甲、乙的溶解度减小,有晶体析出,t1℃时乙的溶解度大于甲,丙的溶解度增大,没有晶体析出,则得到溶液的质量:丙>乙>甲,故选项说法正确。
故选:D。
解析
步骤 1:分析图2中的实验现象
图2中向烧杯中加入NaOH固体,试管中固体由未完全溶解变为完全溶解,说明NaOH溶于水放热,使温度升高,试管内的固体完全溶解,说明该物质的溶解度随着温度的升高而增大,因此图2试管中固体对应的不可能是图1中的丙,因为丙的溶解度随温度升高而减小。
步骤 2:分析t_2℃时甲、乙两饱和溶液中溶质质量
选项B没有指明饱和溶液的质量,因此t_2℃时甲、乙两饱和溶液中溶质质量不一定相等。
步骤 3:分析t_3℃时将40g甲加入到50g水中所得溶液的溶质质量分数
t_3℃时,甲的溶解度为80g,将40g甲加入到50g水中,最多能溶解40g,所得溶液的溶质质量分数为$\frac{40g}{40g+50g}$×100%≈44.4%。
步骤 4:分析将等质量的甲、乙、丙饱和溶液从t_2℃降温到t_1℃,得到溶液的质量
将等质量的甲、乙、丙饱和溶液从t_2℃降温到t_1℃,甲、乙的溶解度减小,有晶体析出,t_1℃时乙的溶解度大于甲,丙的溶解度增大,没有晶体析出,则得到溶液的质量:丙>乙>甲。
图2中向烧杯中加入NaOH固体,试管中固体由未完全溶解变为完全溶解,说明NaOH溶于水放热,使温度升高,试管内的固体完全溶解,说明该物质的溶解度随着温度的升高而增大,因此图2试管中固体对应的不可能是图1中的丙,因为丙的溶解度随温度升高而减小。
步骤 2:分析t_2℃时甲、乙两饱和溶液中溶质质量
选项B没有指明饱和溶液的质量,因此t_2℃时甲、乙两饱和溶液中溶质质量不一定相等。
步骤 3:分析t_3℃时将40g甲加入到50g水中所得溶液的溶质质量分数
t_3℃时,甲的溶解度为80g,将40g甲加入到50g水中,最多能溶解40g,所得溶液的溶质质量分数为$\frac{40g}{40g+50g}$×100%≈44.4%。
步骤 4:分析将等质量的甲、乙、丙饱和溶液从t_2℃降温到t_1℃,得到溶液的质量
将等质量的甲、乙、丙饱和溶液从t_2℃降温到t_1℃,甲、乙的溶解度减小,有晶体析出,t_1℃时乙的溶解度大于甲,丙的溶解度增大,没有晶体析出,则得到溶液的质量:丙>乙>甲。