(2011年福州高二检测)某自来水中含有Ca2+、Mg2+、Na+、K+、HCO、SO、Cl-,长期烧煮上述自来水会在锅炉内形成水垢。锅炉水垢不仅耗费燃料,而且有烧坏锅炉、引起爆炸的危险,因此要定期清除锅炉水垢。已知部分物质20 ℃时的溶解度数据为物质Mg(OH)2CaCO3MgCO3Ca(OH)2CaSO4MgSO4溶解度g/100 g H2O9.0×10-41.5×10-31.0×10-21.7×10-12.1×10-126.7(1)请用化学方程式表示锅炉中的水垢含有Mg(OH)2的原因:________________________________________________________________________________________________________________________________________________。(2)锅炉中的水垢所含有的CaSO4不能直接用酸除去,需要加入试剂X,使其转化为易溶于盐酸的物质Y而除去。试剂X是____________。(填序号)A.NaOH B.NaHCO3C.Na2CO3 D.NaClCaSO4能转化为物质Y的原因是(用文字叙述)_______________________________________________________________________________________________________________。(3)除含CaSO4、Mg(OH)2外,锅炉水垢中还可能含有的物质是(写化学式)_________________ _______________________________________________________。(4)若所用自来水的硬度为33.6度(计算硬度是将Ca2+、Mg2+都看成Ca2+,并将其折算成相当于CaO的质量,通常1 L水中含有10 mg CaO称为1度)。1 t这样的水中相当于含CaO的物质的量为__________(水的密度为1 g/cm3)。(5)水中的Ca2+、Mg2+可以用一定浓度的M溶液进行测定,M与Ca2+、Mg2+都以等物质的量进行反应。现取含Ca2+浓度为0.40 g/L的自来水样10 mL至锥形瓶中进行滴定,达到滴定终点时,用去了浓度为0.01 mol/L的M溶液20.00 mL,则该自来水样中Mg2+的物质的量浓度是____________。解析:(1)加热时水中的Mg(HCO3)2分解,生成的MgCO3溶解度比较大,继续水解产生Mg(OH)2。Mg(HCO3)2MgCO3↓+CO2↑+H2OMgCO3+H2O===Mg(OH)2↓+CO2↑。(2)Na2CO3可以降低水的永久硬度Na2CO3+CaSO4===CaCO3↓+Na2SO4。(4)由信息知33.6度相当于1 L水中含336 mg CaO,1 t水即1000 L,1 t水中含CaO 336×103 mg即336 g,n(CaO)==6 mol。(5)Ca2+浓度为c(Ca2+)==0.01 mol/L,由M~Ca2+(Mg2+)且n(Mg2+)=n(Ca2+),得c(Mg2+)=c(Ca2+)=0.01 mol/L。.
(2011年福州高二检测)某自来水中含有Ca2+、Mg2+、Na+、K+、HCO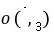 、SO
、SO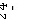 、Cl-,长期烧煮上述自来水会在锅炉内形成水垢。锅炉水垢不仅耗费燃料,而且有烧坏锅炉、引起爆炸的危险,因此要定期清除锅炉水垢。已知部分物质20 ℃时的溶解度数据为
、Cl-,长期烧煮上述自来水会在锅炉内形成水垢。锅炉水垢不仅耗费燃料,而且有烧坏锅炉、引起爆炸的危险,因此要定期清除锅炉水垢。已知部分物质20 ℃时的溶解度数据为
物质
Mg(OH)2
CaCO3
MgCO3
Ca(OH)2
CaSO4
MgSO4
溶解度
g/100 g
H2O
9.0×10-4
1.5×10-3
1.0×10-2
1.7×10-1
2.1×10-1
26.7
(1)请用化学方程式表示锅炉中的水垢含有Mg(OH)2的原因:
________________________________________________________________________
________________________________________________________________________。
(2)锅炉中的水垢所含有的CaSO4不能直接用酸除去,需要加入试剂X,使其转化为易溶于盐酸的物质Y而除去。试剂X是____________。(填序号)
A.NaOH B.NaHCO3
C.Na2CO3 D.NaCl
CaSO4能转化为物质Y的原因是(用文字叙述)_______________________________________
________________________________________________________________________。
(3)除含CaSO4、Mg(OH)2外,锅炉水垢中还可能含有的物质是(写化学式)_________________ _______________________________________________________。
(4)若所用自来水的硬度为33.6度(计算硬度是将Ca2+、Mg2+都看成Ca2+,并将其折算成相当于CaO的质量,通常1 L水中含有10 mg CaO称为1度)。1 t这样的水中相当于含CaO的物质的量为__________(水的密度为1 g/cm3)。
(5)水中的Ca2+、Mg2+可以用一定浓度的M溶液进行测定,M与Ca2+、Mg2+都以等物质的量进行反应。现取含Ca2+浓度为0.40 g/L的自来水样10 mL至锥形瓶中进行滴定,达到滴定终点时,用去了浓度为0.01 mol/L的M溶液20.00 mL,则该自来水样中Mg2+的物质的量浓度是____________。
解析:(1)加热时水中的Mg(HCO3)2分解,生成的MgCO3溶解度比较大,继续水解产生Mg(OH)2。
Mg(HCO3)2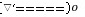 MgCO3↓+CO2↑+H2O
MgCO3↓+CO2↑+H2O
MgCO3+H2O===Mg(OH)2↓+CO2↑。
(2)Na2CO3可以降低水的永久硬度
Na2CO3+CaSO4===CaCO3↓+Na2SO4。
(4)由信息知33.6度相当于1 L水中含336 mg CaO,1 t水即1000 L,1 t水中含CaO 336×103 mg即336 g,n(CaO)=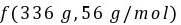 =6 mol。
=6 mol。
(5)Ca2+浓度为c(Ca2+)=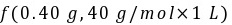 =0.01 mol/L,
=0.01 mol/L,
由M~Ca2+(Mg2+)且n(Mg2+)=n(Ca2+),得c(Mg2+)=c(Ca2+)=0.01 mol/L。
.题目解答
答案
答案:(1)Mg(HCO3)2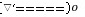 MgCO3↓+H2O+CO2↑,MgCO3+H2O
MgCO3↓+H2O+CO2↑,MgCO3+H2O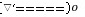 Mg(OH)2↓+CO2↑
Mg(OH)2↓+CO2↑
(2)C 碳酸钙的溶解度远远小于硫酸钙的溶解度
(3)CaCO3、MgCO3等
(4)6 mol (5)0.01 mol/L
.