题目
(15分)下表列出了①~⑨九种元素在周期表中的位置:IA-|||-1 ① ⅡA ⅢA IVA VA VIA VIIA-|||-2 ② ③ ④ ⑧-|||-3 ⑤ ⑥ ⑦ ⑨ 请按要求回答下列问题: (1)元素④的名称是______,元素④在周期表中所处位置______,从元素原子得失电子的角度看,元素④形成的单质具有______性(填“氧化性”或“还原性”). (2)元素⑦的原子结构示意图是______. (3)按气态氢化物的稳定性由弱到强的顺序排列,⑥④⑦的氢化物稳定性:______(写氢化物的化学式). (4)写出元素⑤形成的单质与水反应的化学方程式,并标出转移电子数和方向 . (5)①与⑦能形成一种化合物,用电子式表示该化合物的形成过程______.②NO→NO2实验现象是无色气体变化为红棕色气体,故答案为:无色气体变为红棕色;③二氧化氮和水反应生成一氧化氮和硝酸,反应的化学方程式为:3NO2+H2O=2HNO3+NO,反应中二氧化氮化合价+4价变化为+5价和+2价,氧化剂与还原剂物质的量之比为1;2,故答案为:1:2;(5)图1分析可知X化合价与硝酸相同为+5价,物质类型为氧化物,X化学式为:N2O5,N2O5为酸性氧化物,N2O5+H2O=2HNO3,反应为非氧化还原反应,故答案为:不是;(6)若要将NH3→N2,氮元素化合价-3价变化为0价,氨气做还原剂被氧化。A.O2可以氧化氨气为氮气,故A正确;B.Na是还原剂不能氧化氨气,故B错误;C.NH4Cl中氮元素化合价-3价,不能和氨气反应生成氮气,故C错误;D.NO2和氨气反应做氧化剂,氮元素化合价可以变化为0价,生成氮气,故D正确;故答案为:AD;(7)500L氨气的物质的量为:IA-|||-1 ① ⅡA ⅢA IVA VA VIA VIIA-|||-2 ② ③ ④ ⑧-|||-3 ⑤ ⑥ ⑦ ⑨=22.32mol,溶于水形成1L氨水,c=IA-|||-1 ① ⅡA ⅢA IVA VA VIA VIIA-|||-2 ② ③ ④ ⑧-|||-3 ⑤ ⑥ ⑦ ⑨=IA-|||-1 ① ⅡA ⅢA IVA VA VIA VIIA-|||-2 ② ③ ④ ⑧-|||-3 ⑤ ⑥ ⑦ ⑨=22.3mol/L;氨水吸收过量二氧化硫发生生成亚硫酸氢铵,1体积氨气可以吸收1体积二氧化硫,因此500L氨气最多能吸收SO2500L,故答案为:22.3;500L。点睛:本题考查了氮元素及其化合物的性质。本题的易错点是(7)的计算,一定体积的氨水吸收二氧化硫最多是反应生成酸式盐;另外正确解答本题需要掌握氧化还原反应的基本规律。30. 我国由于硫磺主要依靠进口,所以目前主要以硫铁矿(FeS2)为原料制硫酸,俗称硫铁矿法.Ⅰ.(1)写出硫铁矿与氧气反应的化学方程式:_________________。工业上,该反应在______(填设备名称)中进行.Ⅱ.已知SO3熔点16.83℃、沸点44.8℃.某兴趣小组利用SO2和O2在催化剂V2O5的作用下制备SO3固体.装置如图所示.IA-|||-1 ① ⅡA ⅢA IVA VA VIA VIIA-|||-2 ② ③ ④ ⑧-|||-3 ⑤ ⑥ ⑦ ⑨(2)写出B中催化剂V2O5表面所发生的反应的化学方程式:_______________。(3)学生实验时发现在C装置U形管的右边有白雾生成.改进的办法是______。(4)装置D的作用是吸收尾气,其中干燥管的作用是______.装置D中所装液体试剂可能为______.A.饱和食盐水 B.酒精 C.BaCl2溶液 D.NaOH溶液.(5)接触法生产H2SO4的过程中,对废气、废液、废渣和“废热”的处理正确的是_____。①尾气用氨水处理 ②污水用石灰乳处理 ③废渣用来炼铁、制水泥等 ④将“废热”通过“废热”锅炉产生蒸气发电.A.只有①② B.只有①③④ C.只有①②③ D.全部Ⅲ、在下列用途或反应中,硫酸表现出的性质为:A.高沸点;B.强酸;C.吸水性;D.脱水性;E.强氧化性。试用字母填空:(6)实验室制取氢气_____________。(7)干燥氢气________;(8)浓硫酸与灼热的碳反应______ ;(9)硫酸使蔗糖变黑_______________;
(15分)下表列出了①~⑨九种元素在周期表中的位置: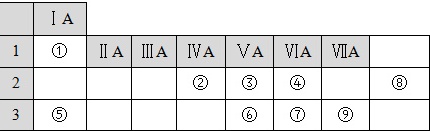 请按要求回答下列问题: (1)元素④的名称是______,元素④在周期表中所处位置______,从元素原子得失电子的角度看,元素④形成的单质具有______性(填“氧化性”或“还原性”). (2)元素⑦的原子结构示意图是______. (3)按气态氢化物的稳定性由弱到强的顺序排列,⑥④⑦的氢化物稳定性:______(写氢化物的化学式). (4)写出元素⑤形成的单质与水反应的化学方程式,并标出转移电子数和方向 . (5)①与⑦能形成一种化合物,用电子式表示该化合物的形成过程______.
请按要求回答下列问题: (1)元素④的名称是______,元素④在周期表中所处位置______,从元素原子得失电子的角度看,元素④形成的单质具有______性(填“氧化性”或“还原性”). (2)元素⑦的原子结构示意图是______. (3)按气态氢化物的稳定性由弱到强的顺序排列,⑥④⑦的氢化物稳定性:______(写氢化物的化学式). (4)写出元素⑤形成的单质与水反应的化学方程式,并标出转移电子数和方向 . (5)①与⑦能形成一种化合物,用电子式表示该化合物的形成过程______.
 请按要求回答下列问题: (1)元素④的名称是______,元素④在周期表中所处位置______,从元素原子得失电子的角度看,元素④形成的单质具有______性(填“氧化性”或“还原性”). (2)元素⑦的原子结构示意图是______. (3)按气态氢化物的稳定性由弱到强的顺序排列,⑥④⑦的氢化物稳定性:______(写氢化物的化学式). (4)写出元素⑤形成的单质与水反应的化学方程式,并标出转移电子数和方向 . (5)①与⑦能形成一种化合物,用电子式表示该化合物的形成过程______.
请按要求回答下列问题: (1)元素④的名称是______,元素④在周期表中所处位置______,从元素原子得失电子的角度看,元素④形成的单质具有______性(填“氧化性”或“还原性”). (2)元素⑦的原子结构示意图是______. (3)按气态氢化物的稳定性由弱到强的顺序排列,⑥④⑦的氢化物稳定性:______(写氢化物的化学式). (4)写出元素⑤形成的单质与水反应的化学方程式,并标出转移电子数和方向 . (5)①与⑦能形成一种化合物,用电子式表示该化合物的形成过程______.②NO→NO2实验现象是无色气体变化为红棕色气体,故答案为:无色气体变为红棕色;
③二氧化氮和水反应生成一氧化氮和硝酸,反应的化学方程式为:3NO2+H2O=2HNO3+NO,反应中二氧化氮化合价+4价变化为+5价和+2价,氧化剂与还原剂物质的量之比为1;2,故答案为:1:2;
(5)图1分析可知X化合价与硝酸相同为+5价,物质类型为氧化物,X化学式为:N2O5,N2O5为酸性氧化物,N2O5+H2O=2HNO3,反应为非氧化还原反应,故答案为:不是;
(6)若要将NH3→N2,氮元素化合价-3价变化为0价,氨气做还原剂被氧化。A.O2可以氧化氨气为氮气,故A正确;B.Na是还原剂不能氧化氨气,故B错误;C.NH4Cl中氮元素化合价-3价,不能和氨气反应生成氮气,故C错误;D.NO2和氨气反应做氧化剂,氮元素化合价可以变化为0价,生成氮气,故D正确;故答案为:AD;
(7)500L氨气的物质的量为: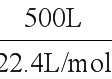 =22.32mol,溶于水形成1L氨水,c=
=22.32mol,溶于水形成1L氨水,c= =
= =22.3mol/L;氨水吸收过量二氧化硫发生生成亚硫酸氢铵,1体积氨气可以吸收1体积二氧化硫,因此500L氨气最多能吸收SO2500L,故答案为:22.3;500L。
=22.3mol/L;氨水吸收过量二氧化硫发生生成亚硫酸氢铵,1体积氨气可以吸收1体积二氧化硫,因此500L氨气最多能吸收SO2500L,故答案为:22.3;500L。
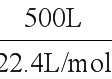 =22.32mol,溶于水形成1L氨水,c=
=22.32mol,溶于水形成1L氨水,c= =
= =22.3mol/L;氨水吸收过量二氧化硫发生生成亚硫酸氢铵,1体积氨气可以吸收1体积二氧化硫,因此500L氨气最多能吸收SO2500L,故答案为:22.3;500L。
=22.3mol/L;氨水吸收过量二氧化硫发生生成亚硫酸氢铵,1体积氨气可以吸收1体积二氧化硫,因此500L氨气最多能吸收SO2500L,故答案为:22.3;500L。点睛:本题考查了氮元素及其化合物的性质。本题的易错点是(7)的计算,一定体积的氨水吸收二氧化硫最多是反应生成酸式盐;另外正确解答本题需要掌握氧化还原反应的基本规律。
30. 我国由于硫磺主要依靠进口,所以目前主要以硫铁矿(FeS2)为原料制硫酸,俗称硫铁矿法.
Ⅰ.(1)写出硫铁矿与氧气反应的化学方程式:_________________。工业上,该反应在______(填设备名称)中进行.
Ⅱ.已知SO3熔点16.83℃、沸点44.8℃.某兴趣小组利用SO2和O2在催化剂V2O5的作用下制备SO3固体.装置如图所示.
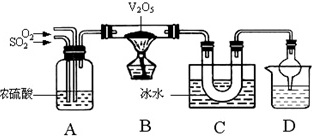
(2)写出B中催化剂V2O5表面所发生的反应的化学方程式:_______________。
(3)学生实验时发现在C装置U形管的右边有白雾生成.改进的办法是______。
(4)装置D的作用是吸收尾气,其中干燥管的作用是______.装置D中所装液体试剂可能为______.
A.饱和食盐水 B.酒精 C.BaCl2溶液 D.NaOH溶液.
(5)接触法生产H2SO4的过程中,对废气、废液、废渣和“废热”的处理正确的是_____。
①尾气用氨水处理 ②污水用石灰乳处理 ③废渣用来炼铁、制水泥等 ④将“废热”通过“废热”锅炉产生蒸气发电.
A.只有①② B.只有①③④ C.只有①②③ D.全部
Ⅲ、在下列用途或反应中,硫酸表现出的性质为:A.高沸点;B.强酸;C.吸水性;D.脱水性;E.强氧化性。试用字母填空:
(6)实验室制取氢气_____________。
(7)干燥氢气________;
(8)浓硫酸与灼热的碳反应______ ;
(9)硫酸使蔗糖变黑_______________;
题目解答
答案
点睛:本题考查了氮元素及其化合物的性质。本题的易错点是(7)的计算,一定体积的氨水吸收二氧化硫最多是反应生成酸式盐;另外正确解答本题需要掌握氧化还原反应的基本规律。
30. 我国由于硫磺主要依靠进口,所以目前主要以硫铁矿(FeS2)为原料制硫酸,俗称硫铁矿法.
Ⅰ.(1)写出硫铁矿与氧气反应的化学方程式:_________________。工业上,该反应在______(填设备名称)中进行.
Ⅱ.已知SO3熔点16.83℃、沸点44.8℃.某兴趣小组利用SO2和O2在催化剂V2O5的作用下制备SO3固体.装置如图所示.

(2)写出B中催化剂V2O5表面所发生的反应的化学方程式:_______________。
(3)学生实验时发现在C装置U形管的右边有白雾生成.改进的办法是______。
(4)装置D的作用是吸收尾气,其中干燥管的作用是______.装置D中所装液体试剂可能为______.
A.饱和食盐水 B.酒精 C.BaCl2溶液 D.NaOH溶液.
(5)接触法生产H2SO4的过程中,对废气、废液、废渣和“废热”的处理正确的是_____。
①尾气用氨水处理 ②污水用石灰乳处理 ③废渣用来炼铁、制水泥等 ④将“废热”通过“废热”锅炉产生蒸气发电.
A.只有①② B.只有①③④ C.只有①②③ D.全部
Ⅲ、在下列用途或反应中,硫酸表现出的性质为:A.高沸点;B.强酸;C.吸水性;D.脱水性;E.强氧化性。试用字母填空:
(6)实验室制取氢气_____________。
(7)干燥氢气________;
(8)浓硫酸与灼热的碳反应______ ;
(9)硫酸使蔗糖变黑_______________;
[答案] (1). 4 FeS 2+11O2  2Fe2O3+8SO2 (2). 沸腾炉 (3). 2SO2+O2
2Fe2O3+8SO2 (2). 沸腾炉 (3). 2SO2+O2 2SO3 (4). CD之间连接一个装有浓硫酸的洗气瓶 (5). 防止倒吸 (6). D (7). D (8). B (9). C (10). E (11). D
2SO3 (4). CD之间连接一个装有浓硫酸的洗气瓶 (5). 防止倒吸 (6). D (7). D (8). B (9). C (10). E (11). D
 2Fe2O3+8SO2 (2). 沸腾炉 (3). 2SO2+O2
2Fe2O3+8SO2 (2). 沸腾炉 (3). 2SO2+O2 2SO3 (4). CD之间连接一个装有浓硫酸的洗气瓶 (5). 防止倒吸 (6). D (7). D (8). B (9). C (10). E (11). D
2SO3 (4). CD之间连接一个装有浓硫酸的洗气瓶 (5). 防止倒吸 (6). D (7). D (8). B (9). C (10). E (11). D[答案] (1). 氩 (2). 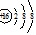 (3).
(3).  O (4). r(O2-)>r(F-)>r(Na+)>r(Al3+) (5). HF>H2O>H2S (6). Al (7). 2Na2SO3+O2=2Na2SO4 (8). 不合理,因为NH3·H2O不是N元素对应的最高价氧化物的水化物
O (4). r(O2-)>r(F-)>r(Na+)>r(Al3+) (5). HF>H2O>H2S (6). Al (7). 2Na2SO3+O2=2Na2SO4 (8). 不合理,因为NH3·H2O不是N元素对应的最高价氧化物的水化物
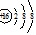 (3).
(3).  O (4). r(O2-)>r(F-)>r(Na+)>r(Al3+) (5). HF>H2O>H2S (6). Al (7). 2Na2SO3+O2=2Na2SO4 (8). 不合理,因为NH3·H2O不是N元素对应的最高价氧化物的水化物
O (4). r(O2-)>r(F-)>r(Na+)>r(Al3+) (5). HF>H2O>H2S (6). Al (7). 2Na2SO3+O2=2Na2SO4 (8). 不合理,因为NH3·H2O不是N元素对应的最高价氧化物的水化物