题目
11.计算下列反应的:(1) (Delta )_(1)(H)_(m)(298.15k) ;(2) Delta (U)_(m)(298.15k) 和(3)298.15K进行-|||-反应进度为1 mol的体积功。-|||-(H)_(4)(g)+4(Cl)_(2)(g)=!=!= C(C)_(4)(l)+4HCl(g) HCl(g)
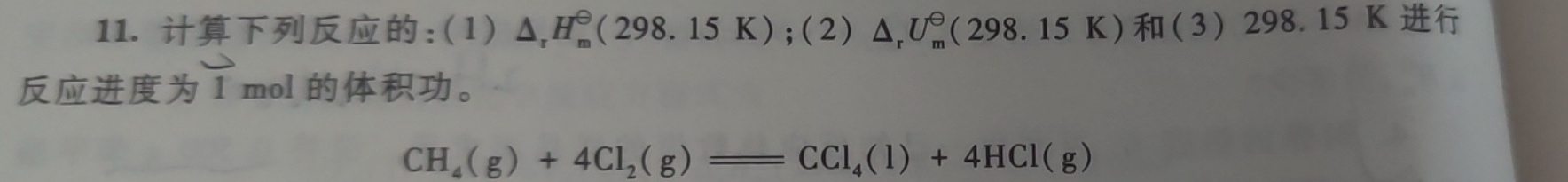
题目解答
答案

解析
步骤 1:计算反应的焓变(△H)
根据标准生成焓(△Hf)的定义,反应的焓变(△H)可以通过反应物和生成物的标准生成焓的差值来计算。对于反应 $C{H}_{4}(g)+4{Cl}_{2}(g)=\!=\!= C{Cl}_{4}(l)+4HCl(g)$,我们有:
$$
\Delta H = \sum \Delta H_f^{o}(生成物) - \sum \Delta H_f^{o}(反应物)
$$
其中,$\Delta H_f^{o}$ 是标准生成焓。根据已知数据,我们有:
$$
\Delta H_f^{o}(C{H}_{4}(g)) = -74.85 kJ/mol
$$
$$
\Delta H_f^{o}(Cl_{2}(g)) = 0 kJ/mol
$$
$$
\Delta H_f^{o}(C{Cl}_{4}(l)) = -139.5 kJ/mol
$$
$$
\Delta H_f^{o}(HCl(g)) = -92.3 kJ/mol
$$
因此,反应的焓变(△H)为:
$$
\Delta H = (-139.5 + 4 \times (-92.3)) - (-74.85 + 4 \times 0) = -429.85 kJ/mol
$$
步骤 2:计算反应的内能变(△U)
反应的内能变(△U)可以通过反应的焓变(△H)和反应的体积功(△V)来计算。对于理想气体,我们有:
$$
\Delta U = \Delta H - \Delta (PV)
$$
其中,$\Delta (PV)$ 是反应的体积功。对于反应 $C{H}_{4}(g)+4{Cl}_{2}(g)=\!=\!= C{Cl}_{4}(l)+4HCl(g)$,反应前后气体的摩尔数变化为:
$$
\Delta n = 4 - 1 = 3
$$
因此,反应的体积功(△V)为:
$$
\Delta (PV) = \Delta n \cdot RT = 3 \cdot 8.314 \cdot 298.15 = 7431.6 J/mol = 7.4316 kJ/mol
$$
因此,反应的内能变(△U)为:
$$
\Delta U = \Delta H - \Delta (PV) = -429.85 - 7.4316 = -437.2816 kJ/mol
$$
步骤 3:计算反应进度为1 mol的体积功
反应进度为1 mol的体积功可以通过反应的体积功(△V)来计算。对于反应 $C{H}_{4}(g)+4{Cl}_{2}(g)=\!=\!= C{Cl}_{4}(l)+4HCl(g)$,反应进度为1 mol的体积功为:
$$
W = -\Delta (PV) = -7.4316 kJ/mol
$$
根据标准生成焓(△Hf)的定义,反应的焓变(△H)可以通过反应物和生成物的标准生成焓的差值来计算。对于反应 $C{H}_{4}(g)+4{Cl}_{2}(g)=\!=\!= C{Cl}_{4}(l)+4HCl(g)$,我们有:
$$
\Delta H = \sum \Delta H_f^{o}(生成物) - \sum \Delta H_f^{o}(反应物)
$$
其中,$\Delta H_f^{o}$ 是标准生成焓。根据已知数据,我们有:
$$
\Delta H_f^{o}(C{H}_{4}(g)) = -74.85 kJ/mol
$$
$$
\Delta H_f^{o}(Cl_{2}(g)) = 0 kJ/mol
$$
$$
\Delta H_f^{o}(C{Cl}_{4}(l)) = -139.5 kJ/mol
$$
$$
\Delta H_f^{o}(HCl(g)) = -92.3 kJ/mol
$$
因此,反应的焓变(△H)为:
$$
\Delta H = (-139.5 + 4 \times (-92.3)) - (-74.85 + 4 \times 0) = -429.85 kJ/mol
$$
步骤 2:计算反应的内能变(△U)
反应的内能变(△U)可以通过反应的焓变(△H)和反应的体积功(△V)来计算。对于理想气体,我们有:
$$
\Delta U = \Delta H - \Delta (PV)
$$
其中,$\Delta (PV)$ 是反应的体积功。对于反应 $C{H}_{4}(g)+4{Cl}_{2}(g)=\!=\!= C{Cl}_{4}(l)+4HCl(g)$,反应前后气体的摩尔数变化为:
$$
\Delta n = 4 - 1 = 3
$$
因此,反应的体积功(△V)为:
$$
\Delta (PV) = \Delta n \cdot RT = 3 \cdot 8.314 \cdot 298.15 = 7431.6 J/mol = 7.4316 kJ/mol
$$
因此,反应的内能变(△U)为:
$$
\Delta U = \Delta H - \Delta (PV) = -429.85 - 7.4316 = -437.2816 kJ/mol
$$
步骤 3:计算反应进度为1 mol的体积功
反应进度为1 mol的体积功可以通过反应的体积功(△V)来计算。对于反应 $C{H}_{4}(g)+4{Cl}_{2}(g)=\!=\!= C{Cl}_{4}(l)+4HCl(g)$,反应进度为1 mol的体积功为:
$$
W = -\Delta (PV) = -7.4316 kJ/mol
$$