题目
理想气体化学反应(g)arrow B(g)+C(g),在恒温下增大总压时,反应物转化率将增大。( )
理想气体化学反应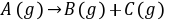 ,在恒温下增大总压时,反应物转化率将增大。( )
,在恒温下增大总压时,反应物转化率将增大。( )
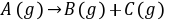 ,在恒温下增大总压时,反应物转化率将增大。( )
,在恒温下增大总压时,反应物转化率将增大。( )题目解答
答案
×
解析
考查要点:本题主要考查化学平衡移动原理(勒沙特列原理)在理想气体反应中的应用,以及压强变化对反应物转化率的影响。
解题核心思路:
- 判断反应前后气体物质的量变化:反应式为$A(g)\rightarrow B(g)+C(g)$,反应物为1 mol气体,生成物为2 mol气体,总物质的量增加。
- 分析压强变化对平衡的影响:在恒温条件下,增大总压强(如通过缩小容器体积实现)会使系统向气体物质的量减少的方向移动。由于本反应生成物总物质的量更大,加压会使平衡逆向移动,导致反应物转化率降低。
- 关键结论:题目中“反应物转化率将增大”的结论与上述分析矛盾,因此判断为错误。
反应物转化率与压强的关系:
- 反应特点:
反应$A(g)\rightarrow B(g)+C(g)$中,反应物总物质的量为1 mol,生成物总物质的量为2 mol,即$\Delta n = 2 - 1 = 1 > 0$。 - 压强变化的影响:
- 增大压强(如缩小容器体积)时,系统会通过减少气体物质的量来“抵消”压强的增加,因此平衡向逆反应方向移动。
- 逆反应方向移动意味着反应物$A$的转化减少,转化率下降。
- 结论:题目中“反应物转化率增大”的说法错误,正确答案为“×”。