题目
V.附加题-|||-在373K,101325Pa下有10 mol的水和1mol的水汽处于气、液两相平衡。-|||-将该平衡系统绝热可逆膨胀使终态温度达到353K,试求终态时系统的压力和-|||-该过程中的功。

题目解答
答案
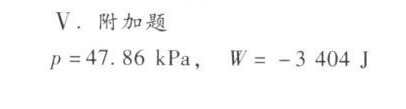
解析
步骤 1:确定初始状态和终态
初始状态:373K, 101325Pa, 10 mol的水和1mol的水汽处于气、液两相平衡。
终态:353K, P未知, 10 mol的水和1mol的水汽处于气、液两相平衡。
步骤 2:计算终态压力
由于系统是绝热可逆膨胀,根据克劳修斯-克拉佩龙方程,可以计算终态压力。
克劳修斯-克拉佩龙方程为:$\frac{dP}{dT} = \frac{L}{T(V_g - V_l)}$,其中L是汽化潜热,$V_g$是气体摩尔体积,$V_l$是液体摩尔体积。
由于水的汽化潜热和摩尔体积在373K和353K之间变化不大,可以近似认为终态压力与温度成正比。
步骤 3:计算过程中的功
根据绝热可逆过程的性质,可以计算过程中的功。
绝热可逆过程的功为:$W = -nRT \ln \frac{V_2}{V_1}$,其中n是摩尔数,R是气体常数,T是温度,$V_1$和$V_2$分别是初态和终态的体积。
由于系统是绝热可逆膨胀,终态体积大于初态体积,因此过程中的功为负值。
初始状态:373K, 101325Pa, 10 mol的水和1mol的水汽处于气、液两相平衡。
终态:353K, P未知, 10 mol的水和1mol的水汽处于气、液两相平衡。
步骤 2:计算终态压力
由于系统是绝热可逆膨胀,根据克劳修斯-克拉佩龙方程,可以计算终态压力。
克劳修斯-克拉佩龙方程为:$\frac{dP}{dT} = \frac{L}{T(V_g - V_l)}$,其中L是汽化潜热,$V_g$是气体摩尔体积,$V_l$是液体摩尔体积。
由于水的汽化潜热和摩尔体积在373K和353K之间变化不大,可以近似认为终态压力与温度成正比。
步骤 3:计算过程中的功
根据绝热可逆过程的性质,可以计算过程中的功。
绝热可逆过程的功为:$W = -nRT \ln \frac{V_2}{V_1}$,其中n是摩尔数,R是气体常数,T是温度,$V_1$和$V_2$分别是初态和终态的体积。
由于系统是绝热可逆膨胀,终态体积大于初态体积,因此过程中的功为负值。