题目
气柜内贮有121.6 kPa,27℃的氯乙烯(C2H3Cl)气体300 m3,若以每小时90 kg 的流量输往使用车间,试问贮存的气体能用多少小时?
气柜内贮有121.6 kPa,27℃的氯乙烯(C2H3Cl)气体300 m3,若以每小时90 kg 的流量输往使用车间,试问贮存的气体能用多少小时?
题目解答
答案
解:假设气体能全部送往车间
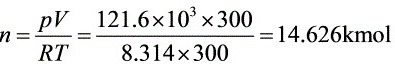
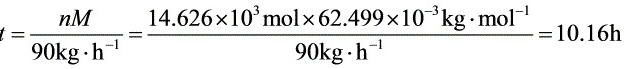
答:贮存的气体能用10.16小时。
解析
考查要点:本题主要考查理想气体状态方程的应用及单位换算,涉及气体物质的量计算、质量与流量的关系。
解题核心思路:
- 利用理想气体状态方程 $PV = nRT$ 计算气体总物质的量 $n$;
- 换算单位(压力、温度、体积需符合气体常数 $R$ 的单位要求);
- 计算气体总质量(根据摩尔数与摩尔质量);
- 求时间(总质量除以流量)。
破题关键点:
- 单位统一:压力需转换为帕斯卡(Pa),温度转换为开尔文(K);
- 分子量计算:氯乙烯(C₂H₃Cl)的分子量需准确计算;
- 公式变形:正确应用 $n = \dfrac{PV}{RT}$ 并代入数据。
步骤1:确定气体总物质的量
根据理想气体状态方程:
$n = \dfrac{PV}{RT}$
其中:
- $P = 121.6 \, \text{kPa} = 121600 \, \text{Pa}$(单位换算);
- $V = 300 \, \text{m}^3$;
- $T = 27^\circ \text{C} = 300 \, \text{K}$;
- $R = 8.314 \, \text{J/(mol·K)}$。
代入数据:
$n = \dfrac{121600 \times 300}{8.314 \times 300} \approx 14.626 \, \text{kmol}$
步骤2:计算气体总质量
氯乙烯的分子量为:
$M = 2 \times 12 + 3 \times 1 + 35.5 = 62.5 \, \text{g/mol} = 0.0625 \, \text{kg/mol}$
总质量:
$m = n \times M = 14.626 \, \text{kmol} \times 62.5 \, \text{kg/kmol} = 914.125 \, \text{kg}$
步骤3:求贮存时间
流量为 $90 \, \text{kg/h}$,则时间:
$t = \dfrac{914.125}{90} \approx 10.16 \, \text{小时}$