(15分)氢能是一种公认的高热值清洁能源,目前世界各国正致力于将高污染高排放的碳能源,过渡成清洁高效低排放的氢能源。氢能应用包括以下三个环节:Ⅰ.氢燃料的制备(1)我国氢气的主要来源是焦炉气制氢,所制得的氢气含有较多的rm CO和rm H_2S,干法脱硫是用氧化铁将硫元素转化为硫化铁。干法脱硫的反应方程式为 。(2)我国科研人员用木屑水蒸气气化制取氢燃料,在一定条件下,反应器中存在如下反应:i.(rm CO_2(g)+C(S) {!=!=!=) 2CO (g)} Delta H_1ii. (rm C(g)+H_2O(g) {!=!=!=) CO(g)+H_2(g)} Delta H_2iii.(rm C(s)+2H_2(g) {!=!=!=) CH_4(g)} Delta H_3iv.(rm CO(g)+H_2O(g) {!=!=!=) CO_2(g)+H_2(g)} Delta H_4v.(rm CH_4(g)+2H_2O(g) {!=!=!=) CO_2(g)+4H_2(g)} Delta H_5①Delta H_5= 。②研究中rm CaO的添加量按照rm CaO中所含的rm Ca和松木屑所含碳的物质的量比确定,在750celsius,控制水蒸气流量为rm 0.1 g/(min·g)下,探究催化剂结果如表所示:((C)_(a))ykparallel n(C) 碳转化率 sqrt (96)-|||-气体体积分数-|||-H2 CO CO2 CH4-|||-0 45.58 22.70 22.37 7.54 61.22-|||-0.5 52.95 21.74 19.11 5.14 56.59-|||-1.0 58.62 22.37 12.60 5.31 61.42由表中数据n(rm (Ca))/n(rm (C))= 时最为合理。n(rm (Ca))/n(rm (C))= 由0到0.5时,rm H_2的体积分数显著增加的原因 。③体系的气化温度不仅对木屑的热解气化反应有影响,而且对rm CaO吸收rm CO_2的能力以及rm CaCO_3的分解反应也有很大影响。实验过程中,控制n(rm (Ca))/n(rm (C))为1.0,水蒸气流量为rm 0.1 g/(min·g),将气化反应温度从700celsius升到850celsius,气化温度对产氢率、产气率的影响如表所示:((C)_(a))ykparallel n(C) 碳转化率 sqrt (96)-|||-气体体积分数-|||-H2 CO CO2 CH4-|||-0 45.58 22.70 22.37 7.54 61.22-|||-0.5 52.95 21.74 19.11 5.14 56.59-|||-1.0 58.62 22.37 12.60 5.31 61.42从产氢率的角度考虑,最佳操作温度是 。随着反应的进行,发现rm CaO的吸收能力逐渐降低,原因是 。Ⅱ.氢燃料的存储(3)将氢气储存于液体燃料中,可以解决氢气的安全高效存储和运输。由于甲醇具有单位体积储氢量高、活化温度低等优点,是理想的液体储氢平台分子。我国学者构建一种双功能结构的催化剂,反应过程中,在催化剂的表面同时活化水和甲醇。下图是甲醇脱氢转化的反应历程(TS表示过渡态)。((C)_(a))ykparallel n(C) 碳转化率 sqrt (96)-|||-气体体积分数-|||-H2 CO CO2 CH4-|||-0 45.58 22.70 22.37 7.54 61.22-|||-0.5 52.95 21.74 19.11 5.14 56.59-|||-1.0 58.62 22.37 12.60 5.31 61.42根据上图判断甲醇脱氢反应中断裂的化学键是 ,该反应的Delta H 0(填“大于”、“等于”或“小于”)。Ⅲ.氢燃料电池实现化学能到电能的转化:(4)一种氢能电池的原理如图:((C)_(a))ykparallel n(C) 碳转化率 sqrt (96)-|||-气体体积分数-|||-H2 CO CO2 CH4-|||-0 45.58 22.70 22.37 7.54 61.22-|||-0.5 52.95 21.74 19.11 5.14 56.59-|||-1.0 58.62 22.37 12.60 5.31 61.42正极的电极反应式为 。在rm Pt电极表面镀一层细小的铂粉,原因是 。
(15分)氢能是一种公认的高热值清洁能源,目前世界各国正致力于将高污染高排放的碳能源,过渡成清洁高效低排放的氢能源。氢能应用包括以下三个环节:
Ⅰ.氢燃料的制备
(1)我国氢气的主要来源是焦炉气制氢,所制得的氢气含有较多的$$\rm CO$$和$$\rm H_2S$$,干法脱硫是用氧化铁将硫元素转化为硫化铁。干法脱硫的反应方程式为 。
(2)我国科研人员用木屑水蒸气气化制取氢燃料,在一定条件下,反应器中存在如下反应:
i.$${\rm CO_2(g)+C(S) \ {\!=\!=\!=} \ 2CO (g)}\ \ \ \ \Delta H_1$$
ii.$$ {\rm C(g)+H_2O(g)\ {\!=\!=\!=} \ CO(g)+H_2(g)}\ \ \ \ \Delta H_2$$
iii.$${\rm C(s)+2H_2(g)\ {\!=\!=\!=} \ CH_4(g)}\ \ \ \ \Delta H_3$$
iv.$${\rm CO(g)+H_2O(g)\ {\!=\!=\!=} \ CO_2(g)+H_2(g)}\ \ \ \ \Delta H_4$$
v.$${\rm CH_4(g)+2H_2O(g)\ {\!=\!=\!=} \ CO_2(g)+4H_2(g)}\ \ \ \ \Delta H_5$$
①$$\Delta H_5=$$ 。
②研究中$$\rm CaO$$的添加量按照$$\rm CaO$$中所含的$$\rm Ca$$和松木屑所含碳的物质的量比确定,在$$750\celsius$$,控制水蒸气流量为$$\rm 0.1\ g/(min·g)$$下,探究催化剂结果如表所示:
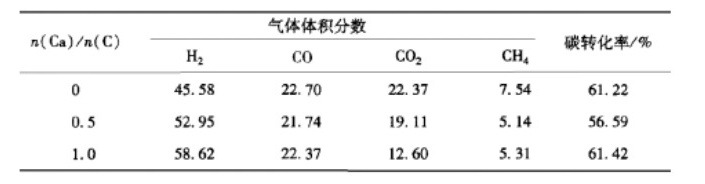
由表中数据$$n{\rm (Ca)}/n{\rm (C)}= $$ 时最为合理。$$n{\rm (Ca)}/n{\rm (C)}= $$由0到0.5时,$$\rm H_2$$的体积分数显著增加的原因 。
③体系的气化温度不仅对木屑的热解气化反应有影响,而且对$$\rm CaO$$吸收$$\rm CO_2$$的能力以及$$\rm CaCO_3$$的分解反应也有很大影响。实验过程中,控制$$n{\rm (Ca)}/n{\rm (C)}$$为1.0,水蒸气流量为$$\rm 0.1\ g/(min·g)$$,将气化反应温度从$$700\celsius$$升到$$850\celsius$$,气化温度对产氢率、产气率的影响如表所示:
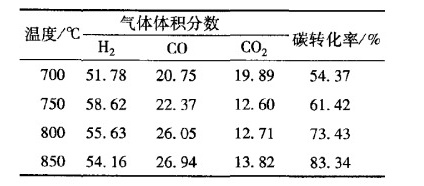
从产氢率的角度考虑,最佳操作温度是 。随着反应的进行,发现$$\rm CaO$$的吸收能力逐渐降低,原因是 。
Ⅱ.氢燃料的存储
(3)将氢气储存于液体燃料中,可以解决氢气的安全高效存储和运输。由于甲醇具有单位体积储氢量高、活化温度低等优点,是理想的液体储氢平台分子。我国学者构建一种双功能结构的催化剂,反应过程中,在催化剂的表面同时活化水和甲醇。下图是甲醇脱氢转化的反应历程(TS表示过渡态)。
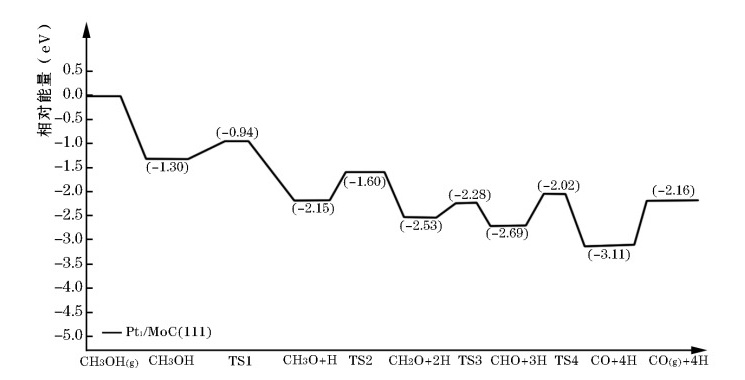
根据上图判断甲醇脱氢反应中断裂的化学键是 ,该反应的$$\Delta H$$ 0(填“大于”、“等于”或“小于”)。
Ⅲ.氢燃料电池实现化学能到电能的转化:
(4)一种氢能电池的原理如图:
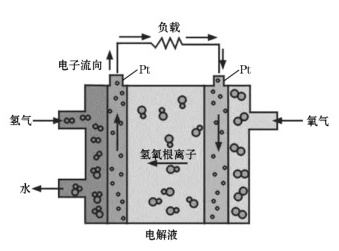
正极的电极反应式为 。在$$\rm Pt$$电极表面镀一层细小的铂粉,原因是 。
题目解答
答案
(除特殊标注外,每空2分)
(1)$$\rm Fe_2O_3 + 3H_2S \ {\!=\!=\!=}\ Fe_2S_3+3H_2O$$
(2)①$$\Delta H_5=2\Delta H_2-\Delta H_1-\Delta H_3 $$或$$\Delta H_5=\Delta H_2+\Delta H_4-\Delta H_3$$或$$\Delta H_5=2\Delta H_4-\Delta H_3+\Delta H_1$$(2分)
②1(1分);$$\rm CaO$$作为$$\rm CO_2 $$的吸收剂,使产气中$$\rm CO_2 $$分压降低,从而使水煤气变换反应平衡向生成$$\rm H_2 $$的方向移动
③$$750\celsius$$(1分); $$\rm CaO$$吸收$$\rm CO_2 $$产生的$$\rm CaCO_3$$附着在$$\rm CaO$$的表面,阻止了$$\rm CaO$$对$$\rm CO_2 $$的进一步吸收
(3)$$\rm O-H$$键和$$\rm C-H$$键(1分);小于(1分)
(4)$$\rm O_2+2H_2O+4e^-\ {\!=\!=\!=} \ 4OH^- $$;铂粉吸附气体的能力强(1分)