题目
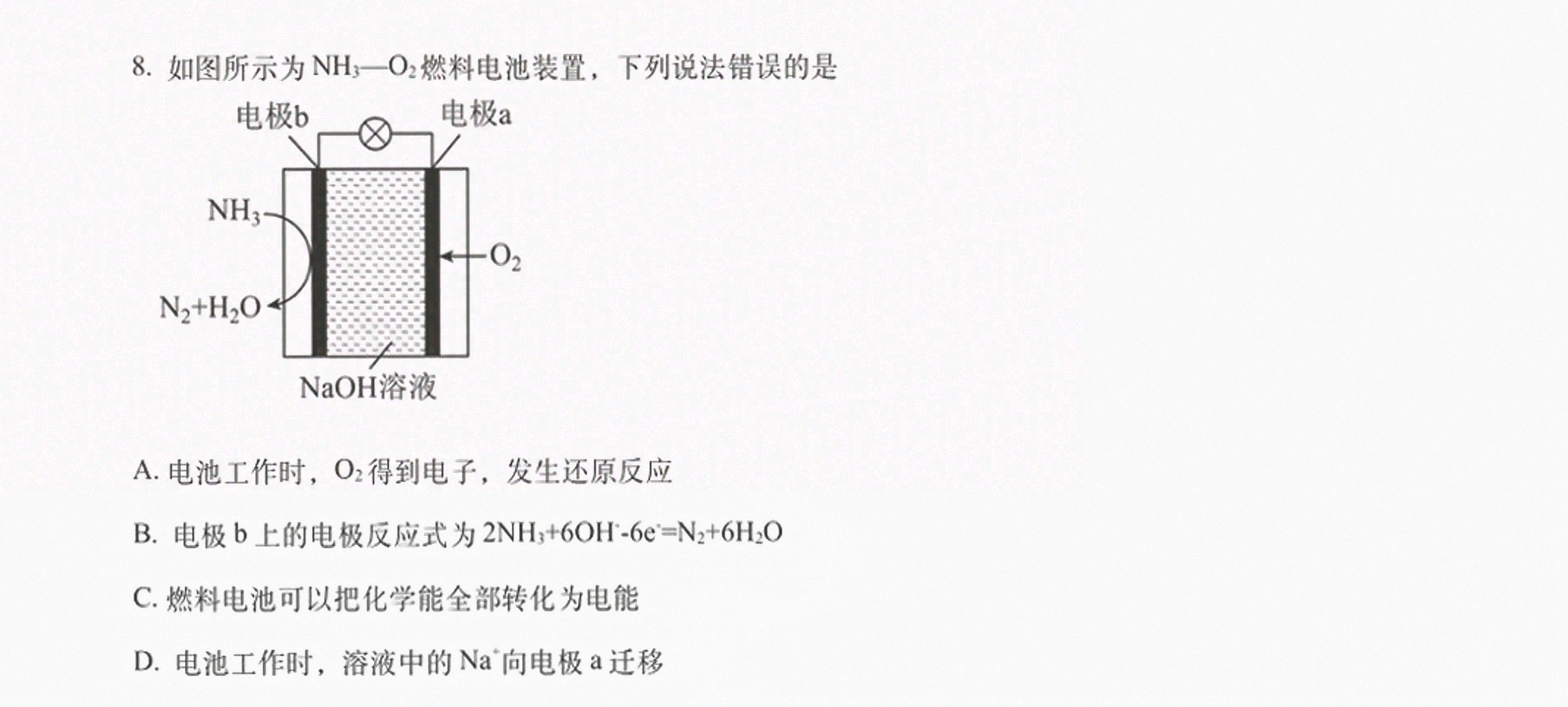
8.如图所示为 (H)_(3)-(O)_(2) 燃料电池装置,下列说法错误的是-|||-电极b 电极a-|||-NH3-|||--O2-|||-_(2)+(H)_(2)O-|||-NaOH溶液-|||-A.电池工作时,O2得到电子,发生还原反应-|||-B.电极b上的电极反应式为 (H)_(3)+6OH-6(e)^-=(N)_(2)+6(H)_(2)O-|||-C.燃料电池可以把化学能全部转化为电能-|||-D.电池工作时,溶液中的 ^+ 向电极a迁移
题目解答
答案

解析
本题考查燃料电池的工作原理,涉及原电池的电极判断、电极反应式书写、离子迁移方向及能量转化效率等知识点。解题核心在于:
- 确定正负极:根据反应物中元素的化合价变化,判断负极(氧化反应)和正极(还原反应)。
- 书写电极反应式:负极反应需体现NH₃被氧化为N₂,正极反应体现O₂被还原为OH⁻。
- 离子迁移规律:阳离子(Na⁺)向正极迁移。
- 能量转化本质:化学能→电能+热能,无法完全转化。
选项分析
A. 电池工作时,O₂得到电子,发生还原反应
- 正极反应:O₂在正极发生还原反应,反应式为:
$O_2 + 4e^- + 2H_2O \rightarrow 4OH^-$
因此A正确。
B. 电极b上的电极反应式为 $2NH_3 + 6OH^- -6e^- \rightarrow N_2 + 6H_2O$
- 负极反应:NH₃在负极被氧化,反应式为:
$2NH_3 + 6OH^- -6e^- \rightarrow N_2 + 6H_2O$
电荷守恒(左边总电荷为 $-6$,右边为 $0$)和原子平衡均成立,因此B正确。
C. 燃料电池可以把化学能全部转化为电能
- 能量守恒:燃料电池中化学能转化为电能和热能,无法完全转化,因此C错误。
D. 电池工作时,溶液中的Na⁺向电极a迁移
- 离子迁移:阳离子(Na⁺)向正极(电极a)迁移,因此D正确。