题目
二氧化铈(CeO2)是一种重要的稀土氧化物。以氟碳铈矿(主要含CeFCO3)为原料制备CeO2的一种工艺流程如:萃取剂 氟洗液 H2O2 NaOH NaClO-|||-H2SO4-|||-CO2盐酸-|||-70% → 氧化-|||-碱碳铈矿 焙烧 匮 圈 → → 反萃取 → 水层 过滤 square 过滤 Ce(OH)4 →CeO2-|||-(含 ^3+-|||-水层 有机层已知:①Ce4+既能与F-结合成[CeFX](4-x)+,也能与SO42-结合成[CeSO4]2+;②在硫酸体系中Ce4+能被萃取剂[(HA)2]萃取,而Ce3+不能。回答下列问题:(1)“氧化焙烧”前需将矿石粉碎成细颗粒,其目的是_____。(2)“酸浸”中会产生大量黄绿色气体,写出CeO2与盐酸反应的离子方程式_____,为避免上述污染,请提出一种决方案:_____。(4)无水AlCl3(183°C升)遇潮湿空气即产生大量白雾,实验室可用下列装置制备。萃取剂 氟洗液 H2O2 NaOH NaClO-|||-H2SO4-|||-CO2盐酸-|||-70% → 氧化-|||-碱碳铈矿 焙烧 匮 圈 → → 反萃取 → 水层 过滤 square 过滤 Ce(OH)4 →CeO2-|||-(含 ^3+-|||-水层 有机层装置 B中盛放饱和NaCl溶液,该装置的主要作用是_________________________。F中试剂的作用是________________;用一件仪器装填适当试剂后也可起到F和G的作用;所装填的试剂为________________。26、(10分)马尾藻和海带中都含丰富的碘,可从中提取碘单质,实验室选取常见的海带设计并进行了以下实验:萃取剂 氟洗液 H2O2 NaOH NaClO-|||-H2SO4-|||-CO2盐酸-|||-70% → 氧化-|||-碱碳铈矿 焙烧 匮 圈 → → 反萃取 → 水层 过滤 square 过滤 Ce(OH)4 →CeO2-|||-(含 ^3+-|||-水层 有机层(1)操作①的名称为___________。A.萃取 B.分液 C.蒸发结晶 D.过滤(2)步骤③中所用的分液漏斗使用前须进行检漏,试简述其操作______。(3)步骤②加入H2O2和H2SO4溶液,反应的离子方程式为___________。27、(12分)某学习小组对人教版教材实验“在200mL烧杯中放入20g蔗糖(C12H22O11),加入适量水,搅拌均匀,然后再加入15mL质量分数为98%浓硫酸,迅速搅拌”进行如下探究;(1)观察现象:蔗糖先变黄,再逐渐变黑,体积膨胀,形成疏松多孔的海绵状黑色物质,同时闻到刺激性气味,按压此黑色物质时,感觉较硬,放在水中呈漂浮状态,同学们由上述现象推测出下列结论:①浓硫酸具有强氧化性 ②浓硫酸具有吸水性 ③浓硫酸具有脱水性④浓硫酸具有酸性 ⑤黑色物质具有强吸附性其中依据不充分的是_________(填序号);(2)为了验证蔗糖与浓硫酸反应生成的气态产物,同学们设计了如下装置:萃取剂 氟洗液 H2O2 NaOH NaClO-|||-H2SO4-|||-CO2盐酸-|||-70% → 氧化-|||-碱碳铈矿 焙烧 匮 圈 → → 反萃取 → 水层 过滤 square 过滤 Ce(OH)4 →CeO2-|||-(含 ^3+-|||-水层 有机层试回答下列问题:①1的A中最好选用下列装置_________(填编号);萃取剂 氟洗液 H2O2 NaOH NaClO-|||-H2SO4-|||-CO2盐酸-|||-70% → 氧化-|||-碱碳铈矿 焙烧 匮 圈 → → 反萃取 → 水层 过滤 square 过滤 Ce(OH)4 →CeO2-|||-(含 ^3+-|||-水层 有机层②1的 B装置所装试剂是_________;D装置中试剂的作用是_________;E装置中发生的现象是_________;③1的A装置中使蔗糖先变黑的化学反应方程式为_________,后体积膨胀的化学方程式为:_________;(3)“萃取”时存在反应:Ce4++n(HA)2萃取剂 氟洗液 H2O2 NaOH NaClO-|||-H2SO4-|||-CO2盐酸-|||-70% → 氧化-|||-碱碳铈矿 焙烧 匮 圈 → → 反萃取 → 水层 过滤 square 过滤 Ce(OH)4 →CeO2-|||-(含 ^3+-|||-水层 有机层Ce·(H2n-4A2n)+4H+。实验室中萃取时用到的主要玻璃仪器名称为_____。(4)“反萃取”中,在稀硫酸和H2O2的作用下CeO2转化为Ce3+,H2O2在该反应中作_____(填“催化剂”、“氧化剂”或“还原剂”),每有1molH2O2参加反应,转移电子物质的量为_____。(5)“氧化”步骤的化学方程式为_____。(6)取上述流程得到的CeO2产品0.50g,加硫酸溶后,用0.10mol/L FeSO4标准溶液滴定至终点时(铈被还原为Ce3+,其他杂质均不参加反应),消耗25.00mL标准溶液。该产品中CeO2的质量分数为_____(Ce的相对原子质量为140)。
二氧化铈(CeO2)是一种重要的稀土氧化物。以氟碳铈矿(主要含CeFCO3)为原料制备CeO2的一种工艺流程如:
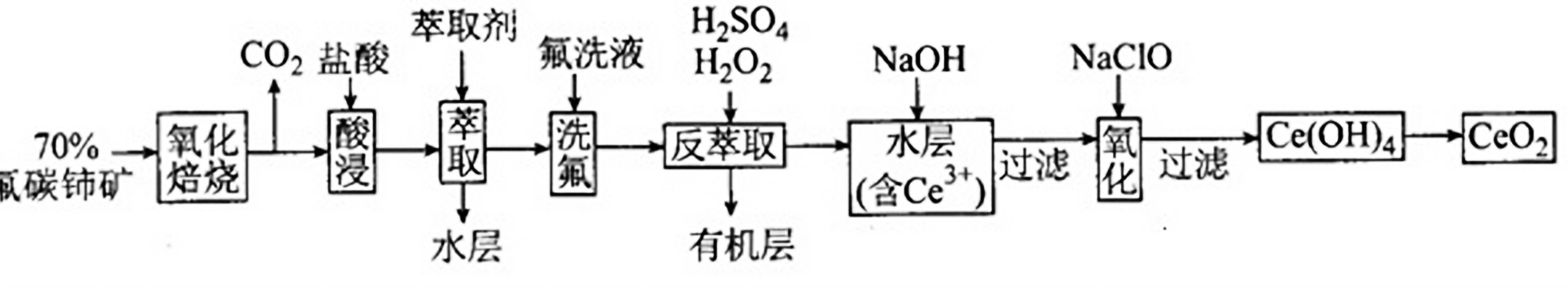
已知:①Ce4+既能与F-结合成[CeFX](4-x)+,也能与SO42-结合成[CeSO4]2+;
②在硫酸体系中Ce4+能被萃取剂[(HA)2]萃取,而Ce3+不能。
回答下列问题:
(1)“氧化焙烧”前需将矿石粉碎成细颗粒,其目的是_____。
(2)“酸浸”中会产生大量黄绿色气体,写出CeO2与盐酸反应的离子方程式_____,为避免上述污染,请提出一种决方案:_____。
(4)无水AlCl3(183°C升)遇潮湿空气即产生大量白雾,实验室可用下列装置制备。
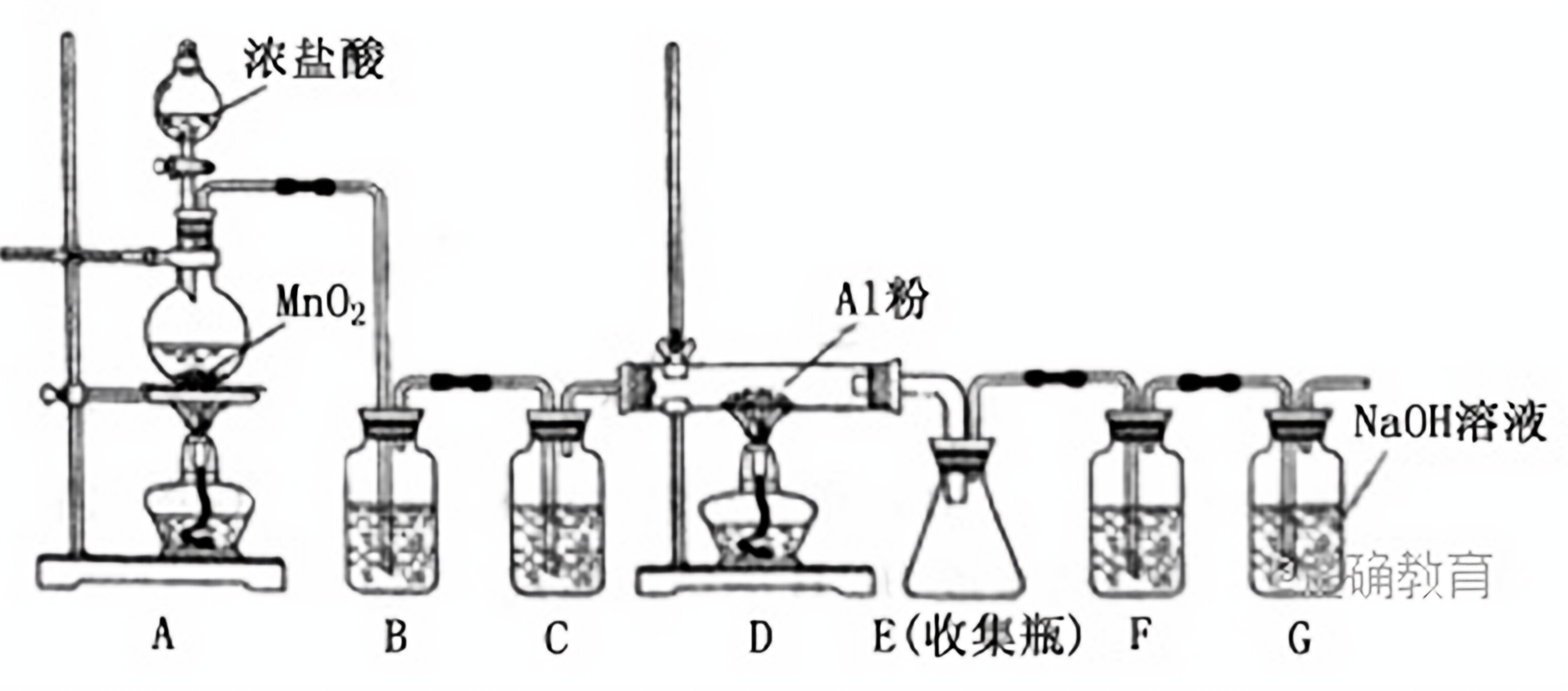
装置 B中盛放饱和NaCl溶液,该装置的主要作用是_________________________。F中试剂的作用是________________;用一件仪器装填适当试剂后也可起到F和G的作用;所装填的试剂为________________。
26、(10分)马尾藻和海带中都含丰富的碘,可从中提取碘单质,实验室选取常见的海带设计并进行了以下实验:
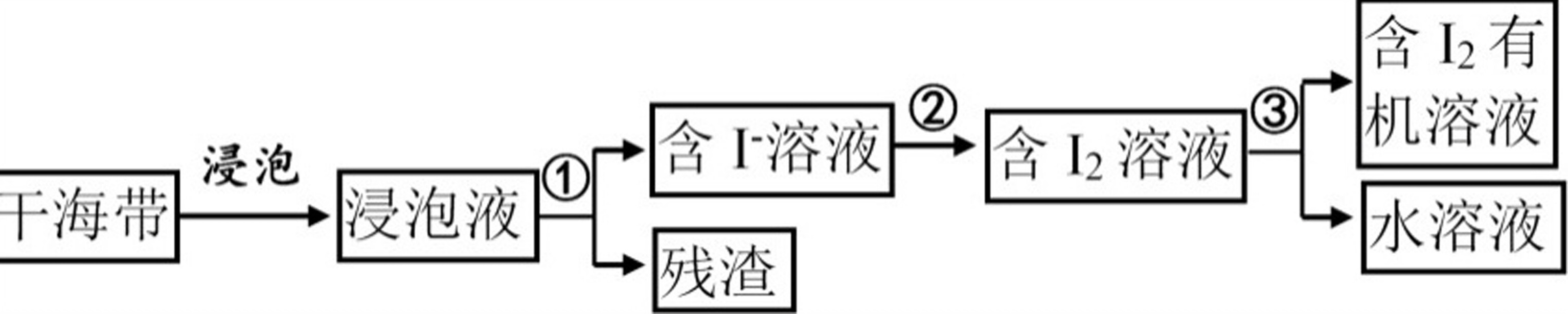
(1)操作①的名称为___________。
A.萃取 B.分液 C.蒸发结晶 D.过滤
(2)步骤③中所用的分液漏斗使用前须进行检漏,试简述其操作______。
(3)步骤②加入H2O2和H2SO4溶液,反应的离子方程式为___________。
27、(12分)某学习小组对人教版教材实验“在200mL烧杯中放入20g蔗糖(C12H22O11),加入适量水,搅拌均匀,然后再加入15mL质量分数为98%浓硫酸,迅速搅拌”进行如下探究;
(1)观察现象:蔗糖先变黄,再逐渐变黑,体积膨胀,形成疏松多孔的海绵状黑色物质,同时闻到刺激性气味,按压此黑色物质时,感觉较硬,放在水中呈漂浮状态,同学们由上述现象推测出下列结论:
①浓硫酸具有强氧化性 ②浓硫酸具有吸水性 ③浓硫酸具有脱水性④浓硫酸具有酸性 ⑤黑色物质具有强吸附性
其中依据不充分的是_________(填序号);
(2)为了验证蔗糖与浓硫酸反应生成的气态产物,同学们设计了如下装置:
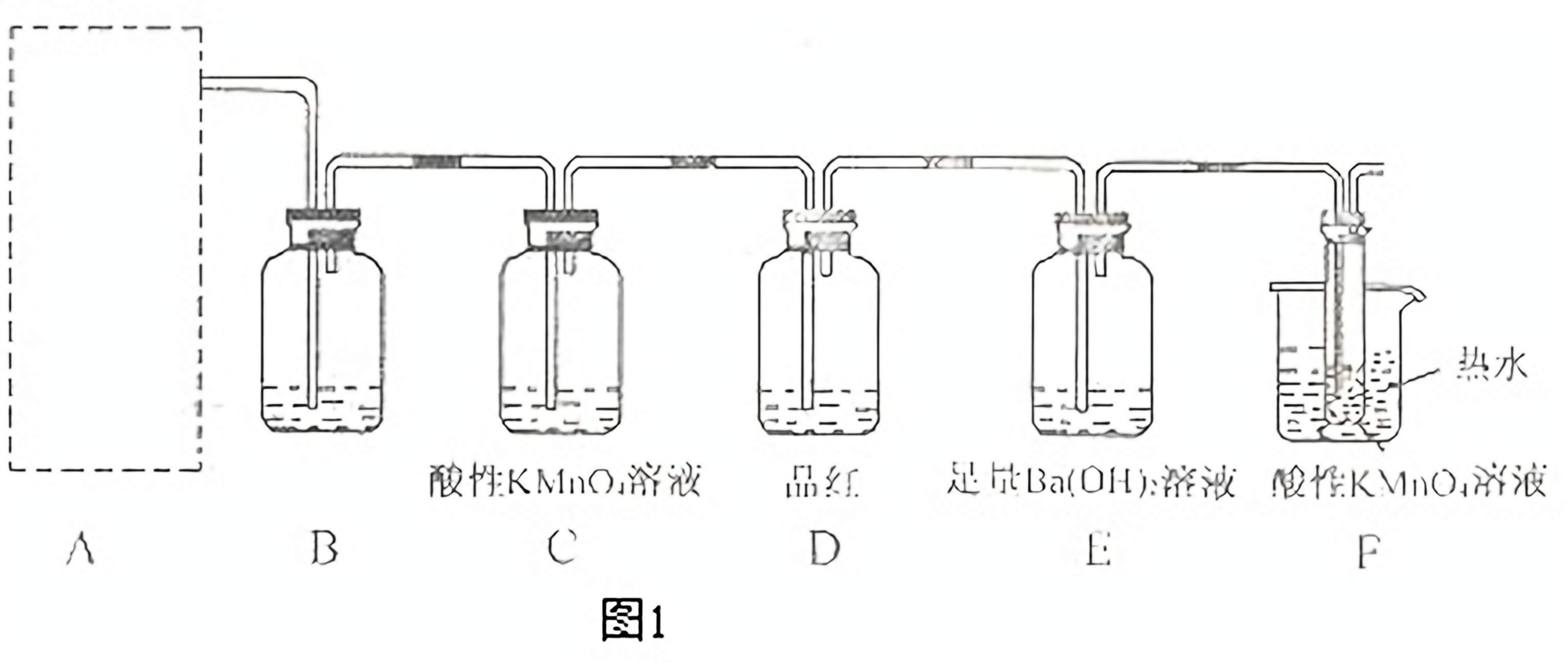
试回答下列问题:
①1的A中最好选用下列装置_________(填编号);
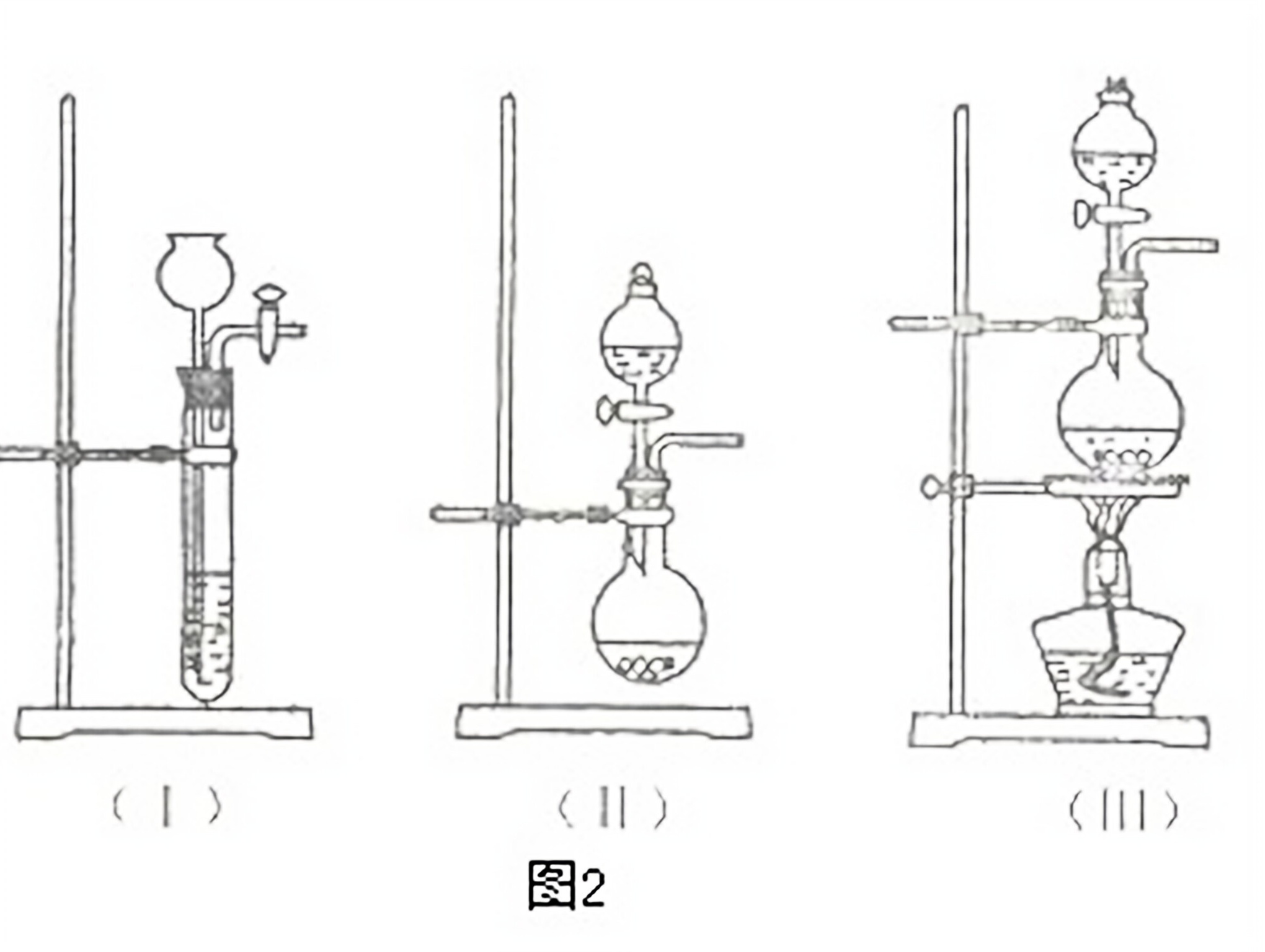
②1的 B装置所装试剂是_________;D装置中试剂的作用是_________;E装置中发生的现象是_________;
③1的A装置中使蔗糖先变黑的化学反应方程式为_________,后体积膨胀的化学方程式为:_________;
(3)“萃取”时存在反应:Ce4++n(HA)2 Ce·(H2n-4A2n)+4H+。实验室中萃取时用到的主要玻璃仪器名称为_____。
Ce·(H2n-4A2n)+4H+。实验室中萃取时用到的主要玻璃仪器名称为_____。
 Ce·(H2n-4A2n)+4H+。实验室中萃取时用到的主要玻璃仪器名称为_____。
Ce·(H2n-4A2n)+4H+。实验室中萃取时用到的主要玻璃仪器名称为_____。(4)“反萃取”中,在稀硫酸和H2O2的作用下CeO2转化为Ce3+,H2O2在该反应中作_____(填“催化剂”、“氧化剂”或“还原剂”),每有1molH2O2参加反应,转移电子物质的量为_____。
(5)“氧化”步骤的化学方程式为_____。
(6)取上述流程得到的CeO2产品0.50g,加硫酸溶后,用0.10mol/L FeSO4标准溶液滴定至终点时(铈被还原为Ce3+,其他杂质均不参加反应),消耗25.00mL标准溶液。该产品中CeO2的质量分数为_____(Ce的相对原子质量为140)。
题目解答
答案
增大固体与空气的接触面积,增大反应速率,提高原料利用率2CeO2+2Cl-+8H+=2Ce3++Cl2↑+4H2O将HCl(盐酸)改用H2SO4酸浸分液漏斗还原剂2mol2Ce(OH)3+NaClO+H2O=2Ce(OH)4+NaCl86%