题目
木炭作为还原剂用于金属冶炼有几千年历史,教材用如图实验介绍这一知识。木炭粉和氧化铜-|||-网罩-|||-澄清-|||-石灰水-|||-① ② ③(1)木炭与氧化铜反应的化学方程式是 ____ 。(2)酒精灯火焰处加有铁丝网罩,其作用是 ____ 。(3)上图实验现象为 ____ 。(填字母序号)A.①中黑色粉末变成红色B.②中澄清的石灰水变浑浊C.①中红色粉末变成黑色D.生成二氧化碳气体(4)由于试管中有空气,实验时应注意:①混合物需进行预热,除了使试管受热均匀外,另外的目的是 ____ 。②实验结束时,可先用弹簧夹夹紧橡皮管,再熄灭酒精灯,这样做的目的除了防止石灰水倒吸入热的试管,使试管炸裂外,还可以防止 ____ 。【发现问题】实验过程中发现有的小组“黑色固体变红色”这一实验现象不明显。小组同学对此异常现象进行如下探究。【知识回忆】碳和氧化铜反应,理论上碳和氧化铜的质量比为 ____ 。【作出猜想】产生异常现象可能与所取用炭粉和氧化铜的质量比有关。注意:若答对以下问题奖励3分,化学总得分不超过40分。【实验探究】小组同学用总质量相同但质量比不同的炭粉和氧化铜的混合物(不考虑其中杂质),分别进行实验,部分实验现象记录如下: 实验序号 m(C):m(CuO) 实验后A处试管中固体颜色 C处导管口的现象 1 1:8 红色固体中有少量黑色固体 尾气燃烧 2 1:9 红色固体中有较少量黑色固体 尾气燃烧 3 1:10 红色固体中有很少量黑色固体 尾气不燃烧 4 1:11 红色固体中有极少量黑色固体 ____ 5 1:12 红色固体中无黑色固体 尾气不燃烧 6 1:13 红色固体中有较多黑色固体 尾气不燃烧 【交流讨论】(1)推测实验4中“C处导管口的现象”是 ____ 。(2)上述探究可得出,实验时所用炭粉和氧化铜的质量比控制在1:10~1:12之间,可观察到黑色固体明显变红,同时还可减少 ____ (填化学式)排放,防止空气污染。【反思评价】分析发现,实验5中m(C):m(CuO)比值与理论值不符,实验后却无黑色固体残留。请用化学方程式解释实验中过量的黑色固体消失的原因: ____ (写一个即可)。
木炭作为还原剂用于金属冶炼有几千年历史,教材用如图实验介绍这一知识。
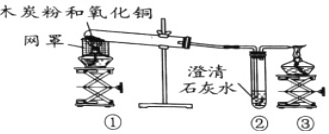
(1)木炭与氧化铜反应的化学方程式是 ____ 。
(2)酒精灯火焰处加有铁丝网罩,其作用是 ____ 。
(3)上图实验现象为 ____ 。(填字母序号)
A.①中黑色粉末变成红色
B.②中澄清的石灰水变浑浊
C.①中红色粉末变成黑色
D.生成二氧化碳气体
(4)由于试管中有空气,实验时应注意:
①混合物需进行预热,除了使试管受热均匀外,另外的目的是 ____ 。
②实验结束时,可先用弹簧夹夹紧橡皮管,再熄灭酒精灯,这样做的目的除了防止石灰水倒吸入热的试管,使试管炸裂外,还可以防止 ____ 。
【发现问题】实验过程中发现有的小组“黑色固体变红色”这一实验现象不明显。小组同学对此异常现象进行如下探究。
【知识回忆】碳和氧化铜反应,理论上碳和氧化铜的质量比为 ____ 。
【作出猜想】产生异常现象可能与所取用炭粉和氧化铜的质量比有关。
注意:若答对以下问题奖励3分,化学总得分不超过40分。
【实验探究】小组同学用总质量相同但质量比不同的炭粉和氧化铜的混合物(不考虑其中杂质),分别进行实验,部分实验现象记录如下:
【交流讨论】
(1)推测实验4中“C处导管口的现象”是 ____ 。
(2)上述探究可得出,实验时所用炭粉和氧化铜的质量比控制在1:10~1:12之间,可观察到黑色固体明显变红,同时还可减少 ____ (填化学式)排放,防止空气污染。
【反思评价】分析发现,实验5中m(C):m(CuO)比值与理论值不符,实验后却无黑色固体残留。请用化学方程式解释实验中过量的黑色固体消失的原因: ____ (写一个即可)。

(1)木炭与氧化铜反应的化学方程式是 ____ 。
(2)酒精灯火焰处加有铁丝网罩,其作用是 ____ 。
(3)上图实验现象为 ____ 。(填字母序号)
A.①中黑色粉末变成红色
B.②中澄清的石灰水变浑浊
C.①中红色粉末变成黑色
D.生成二氧化碳气体
(4)由于试管中有空气,实验时应注意:
①混合物需进行预热,除了使试管受热均匀外,另外的目的是 ____ 。
②实验结束时,可先用弹簧夹夹紧橡皮管,再熄灭酒精灯,这样做的目的除了防止石灰水倒吸入热的试管,使试管炸裂外,还可以防止 ____ 。
【发现问题】实验过程中发现有的小组“黑色固体变红色”这一实验现象不明显。小组同学对此异常现象进行如下探究。
【知识回忆】碳和氧化铜反应,理论上碳和氧化铜的质量比为 ____ 。
【作出猜想】产生异常现象可能与所取用炭粉和氧化铜的质量比有关。
注意:若答对以下问题奖励3分,化学总得分不超过40分。
【实验探究】小组同学用总质量相同但质量比不同的炭粉和氧化铜的混合物(不考虑其中杂质),分别进行实验,部分实验现象记录如下:
| 实验序号 | m(C):m(CuO) | 实验后A处试管中固体颜色 | C处导管口的现象 |
| 1 | 1:8 | 红色固体中有少量黑色固体 | 尾气燃烧 |
| 2 | 1:9 | 红色固体中有较少量黑色固体 | 尾气燃烧 |
| 3 | 1:10 | 红色固体中有很少量黑色固体 | 尾气不燃烧 |
| 4 | 1:11 | 红色固体中有极少量黑色固体 | ____ |
| 5 | 1:12 | 红色固体中无黑色固体 | 尾气不燃烧 |
| 6 | 1:13 | 红色固体中有较多黑色固体 | 尾气不燃烧 |
(1)推测实验4中“C处导管口的现象”是 ____ 。
(2)上述探究可得出,实验时所用炭粉和氧化铜的质量比控制在1:10~1:12之间,可观察到黑色固体明显变红,同时还可减少 ____ (填化学式)排放,防止空气污染。
【反思评价】分析发现,实验5中m(C):m(CuO)比值与理论值不符,实验后却无黑色固体残留。请用化学方程式解释实验中过量的黑色固体消失的原因: ____ (写一个即可)。
题目解答
答案
解:(1)碳与氧化铜反应在高温条件下反应生成铜和二氧化碳,该反应的化学方程式:C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑,故答案为:C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑;
(2)酒精灯火焰处加有铁丝网罩,其作用是:聚集火焰,提高火焰温度;故答案为:聚集火焰,提高火焰温度;
(3)A、碳与氧化铜反应在高温条件下反应生成铜和二氧化碳,①中黑色粉末变成红色,故A正确;
B、二氧化碳与氢氧化钙反应生成碳酸钙和水,②中澄清的石灰水变浑浊,故B正确;
C、碳与氧化铜反应在高温条件下反应生成铜和二氧化碳,①中黑色粉末变成红色,故C错误;
D、描述实验现象不能出现生成物的名称,故D错误;
故答案为:AB;
(4)①混合物需进行预热,除了使试管受热均匀外,另外的目的是排出试管内的一部分空气,排除装置内的空气对实验造成影响;故答案为:排出试管内的一部分空气;
②实验结束时,可先用弹簧夹夹紧橡皮管,再熄灭酒精灯,这样做的目的除了防止石灰水倒吸入热的试管,使试管炸裂外,还可以防止铜被重新氧化,因为铜在加热的条件下与氧气反应生成氧化铜;故答案为:铜被重新氧化;
[知识回忆]碳和氧化铜反应的化学方程式为:C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑,每12份质量的碳与160份质量的氧化铜在高温的条件下完全反应,碳和氧化铜的质量比=12:160=3:40;故答案为:3:40;
[交流讨论](1)总质量相同但质量比不同的炭粉和氡化铜的混合物,分别进行实验,由表可知:随着氧化铜比例增大,生成的尾气不再燃烧,推测实验4、5中“C处导管口的现象”是尾气不燃烧;故答案为:尾气不燃烧;
(2)上述探究可得出,实验时所用炭粉和氧化铜的质量比控制在1:10~1:12之间,可观察到黑色固体明显变红,此时生成的尾气不燃烧,此时一氧化碳生成量减少,同时还可减少CO排放,防止空气污染;故答案为:CO;
[反思评价]分析发现,实验5中m(C):m(CuO)比值与理论值不符,实验后却无黑色固体残留,说明碳与二氧化碳在高温条件下反应生成一氧化碳,该反应的化学方程式:C+CO2$\frac{\underline{\;高温\;}}{\;}$2CO,故答案为:C+CO2$\frac{\underline{\;高温\;}}{\;}$2CO。
(2)酒精灯火焰处加有铁丝网罩,其作用是:聚集火焰,提高火焰温度;故答案为:聚集火焰,提高火焰温度;
(3)A、碳与氧化铜反应在高温条件下反应生成铜和二氧化碳,①中黑色粉末变成红色,故A正确;
B、二氧化碳与氢氧化钙反应生成碳酸钙和水,②中澄清的石灰水变浑浊,故B正确;
C、碳与氧化铜反应在高温条件下反应生成铜和二氧化碳,①中黑色粉末变成红色,故C错误;
D、描述实验现象不能出现生成物的名称,故D错误;
故答案为:AB;
(4)①混合物需进行预热,除了使试管受热均匀外,另外的目的是排出试管内的一部分空气,排除装置内的空气对实验造成影响;故答案为:排出试管内的一部分空气;
②实验结束时,可先用弹簧夹夹紧橡皮管,再熄灭酒精灯,这样做的目的除了防止石灰水倒吸入热的试管,使试管炸裂外,还可以防止铜被重新氧化,因为铜在加热的条件下与氧气反应生成氧化铜;故答案为:铜被重新氧化;
[知识回忆]碳和氧化铜反应的化学方程式为:C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑,每12份质量的碳与160份质量的氧化铜在高温的条件下完全反应,碳和氧化铜的质量比=12:160=3:40;故答案为:3:40;
[交流讨论](1)总质量相同但质量比不同的炭粉和氡化铜的混合物,分别进行实验,由表可知:随着氧化铜比例增大,生成的尾气不再燃烧,推测实验4、5中“C处导管口的现象”是尾气不燃烧;故答案为:尾气不燃烧;
(2)上述探究可得出,实验时所用炭粉和氧化铜的质量比控制在1:10~1:12之间,可观察到黑色固体明显变红,此时生成的尾气不燃烧,此时一氧化碳生成量减少,同时还可减少CO排放,防止空气污染;故答案为:CO;
[反思评价]分析发现,实验5中m(C):m(CuO)比值与理论值不符,实验后却无黑色固体残留,说明碳与二氧化碳在高温条件下反应生成一氧化碳,该反应的化学方程式:C+CO2$\frac{\underline{\;高温\;}}{\;}$2CO,故答案为:C+CO2$\frac{\underline{\;高温\;}}{\;}$2CO。