Delta (U)_(T)=0的应用条件为的应用条件为( )A理想气体的恒温过程B孤立体系C恒温恒压,非体积功为零的封闭体系D不作非体积功,无化学反应,均相,封闭体系中的可逆过程E可逆过程
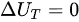 的应用条件为的应用条件为( )
的应用条件为的应用条件为( )
A理想气体的恒温过程
B孤立体系
C恒温恒压,非体积功为零的封闭体系
D不作非体积功,无化学反应,均相,封闭体系中的可逆过程
E可逆过程
题目解答
答案
A选项:理想气体的恒温过程。在恒温过程中,虽然温度不变,但并不意味着内能变化量为零。因为理想气体的内能只与温度有关,但这并不意味着在任何条件下内能都不变。例如,在恒温恒压且非体积功不为零的情况下,系统可能通过做功与外界交换能量,导致内能变化。因此,A选项错误。
B选项:孤立体系。孤立体系是指与外界既没有物质交换也没有能量交换的系统。但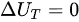 并不特指孤立体系,因为即使不是孤立体系,只要满足一定条件(如可逆过程且非体积功为零),系统的内能变化量也可以为零。因此,B选项错误。
并不特指孤立体系,因为即使不是孤立体系,只要满足一定条件(如可逆过程且非体积功为零),系统的内能变化量也可以为零。因此,B选项错误。
C选项:恒温恒压,非体积功为零的封闭体系。这个选项虽然提到了恒温恒压和封闭体系,但非体积功为零并不是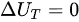 的必要条件。在恒温恒压下,只要系统没有发生相变、化学反应等导致内能变化的过程,且非体积功为零(或可忽略不计),那么系统的内能变化量才可能为零。但这里的关键是“可能”,而不是“一定”,因为还需要考虑其他可能影响内能的因素。因此,C选项的表述不够准确,错误。
的必要条件。在恒温恒压下,只要系统没有发生相变、化学反应等导致内能变化的过程,且非体积功为零(或可忽略不计),那么系统的内能变化量才可能为零。但这里的关键是“可能”,而不是“一定”,因为还需要考虑其他可能影响内能的因素。因此,C选项的表述不够准确,错误。
D选项:不作非体积功,无化学反应,均相,封闭体系中的可逆过程。这个选项完全符合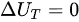 的应用条件。在可逆过程中,系统总是趋向于恢复到原来的状态,因此内能变化量为零。同时,由于不作非体积功、无化学反应、均相且封闭,这些因素都保证了系统内部没有发生导致内能变化的过程。因此,D选项正确。
的应用条件。在可逆过程中,系统总是趋向于恢复到原来的状态,因此内能变化量为零。同时,由于不作非体积功、无化学反应、均相且封闭,这些因素都保证了系统内部没有发生导致内能变化的过程。因此,D选项正确。
E选项:可逆过程。虽然可逆过程是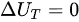 的一个可能条件,但它并不是充分条件。因为即使过程是可逆的,如果系统发生了非体积功、化学反应或相变等导致内能变化的过程,那么内能变化量也可能不为零。因此,E选项错误。
的一个可能条件,但它并不是充分条件。因为即使过程是可逆的,如果系统发生了非体积功、化学反应或相变等导致内能变化的过程,那么内能变化量也可能不为零。因此,E选项错误。
答案是D。
解析
考查要点:本题主要考查热力学中内能变化($\Delta U$)为零的条件,涉及热力学基本概念和不同过程的特点。
解题核心思路:
- 明确内能变化的决定因素:内能是状态函数,其变化由系统的状态(如温度、物质组成、相态等)决定。
- 分析选项中的过程特点:需判断选项中描述的过程是否满足“无内能变化”的条件,即系统内部无能量交换、无化学反应、无相变等。
- 排除干扰项:注意区分“孤立体系”“恒温过程”“可逆过程”等概念的差异,明确哪些条件能严格保证$\Delta U=0$。
破题关键点:
- 封闭体系:排除物质交换的影响。
- 无化学反应与相变:确保物质组成和相态不变。
- 不作非体积功:排除非体积功对能量的影响。
- 可逆过程:保证过程的可逆性,使系统始终处于平衡状态。
选项分析
A. 理想气体的恒温过程
- 理想气体的内能仅与温度有关,恒温时$\Delta U=0$。
- 但:若过程伴随非体积功(如电功、搅拌功等),系统仍可能与外界交换能量,导致内能变化。
- 结论:条件不充分,错误。
B. 孤立体系
- 孤立体系与外界无能量和物质交换,$\Delta U=0$是必然结果。
- 但:题目要求的是“应用条件”,而非孤立体系的特性。
- 结论:与题意无关,错误。
C. 恒温恒压,非体积功为零的封闭体系
- 恒温下理想气体$\Delta U=0$,但若存在相变或化学反应,内能仍可能变化。
- 关键缺失:未排除化学反应或相变的可能。
- 结论:条件不严格,错误。
D. 不作非体积功,无化学反应,均相,封闭体系中的可逆过程
- 封闭体系:无物质交换。
- 无化学反应与相变:物质组成和相态固定。
- 不作非体积功:排除非体积功对能量的影响。
- 可逆过程:系统始终处于平衡状态,能量交换可逆。
- 结论:所有条件共同作用,严格保证$\Delta U=0$,正确。
E. 可逆过程
- 可逆过程仅保证能量交换的可逆性,若伴随化学反应或非体积功,$\Delta U$仍可能不为零。
- 结论:条件不充分,错误。