13.称取肉样8.00g于250mL锥形瓶,加入定量无氨蒸馏水,处理定容得到肉样溶液100.0mL,吸取-|||-5.00mL肉样溶液,经蒸馏等处理后,得到接收液,加入甲基红指示剂,用 .01105molcdot (L)^-1 的HCl滴-|||-至终点,消耗HCl为6.50mL。用5.00mL无氨蒸馏水做空白试验、消耗0.50mL的HCl,求肉样中挥-|||-发性盐基氮含量。以 cdot (g)^-1 表示。(MN:14.00)

题目解答
答案
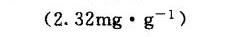
解析
考查要点:本题主要考查挥发性盐基氮的测定原理及计算,涉及酸碱滴定、空白校正、稀释倍数的处理等知识点。
解题核心思路:
- 空白校正:用样品消耗的HCl体积减去空白消耗体积,得到实际反应的HCl体积。
- 物质的量计算:根据HCl的浓度和体积计算n(HCl),进而求出n(NH₃)。
- 氮含量换算:将NH₃的物质的量转换为氮的物质的量,结合摩尔质量计算质量。
- 稀释倍数处理:根据取样体积和定容体积,计算原样品中的总氮含量,最终换算为mg/g单位。
破题关键点:
- 扣除空白:空白试验用于消除试剂和操作中的误差。
- 稀释关系:5.00mL肉样溶液代表原100.00mL溶液中的氮含量,需按比例放大。
步骤1:计算净消耗HCl体积
样品消耗HCl体积:$V_{\text{样}} = 6.50\ \text{mL}$
空白消耗HCl体积:$V_{\text{空}} = 0.50\ \text{mL}$
净消耗HCl体积:
$V_{\text{净}} = V_{\text{样}} - V_{\text{空}} = 6.50\ \text{mL} - 0.50\ \text{mL} = 6.00\ \text{mL}$
步骤2:计算HCl的物质的量
HCl浓度:$c_{\text{HCl}} = 0.01105\ \text{mol/L}$
HCl体积:$V_{\text{HCl}} = 6.00\ \text{mL} = 0.00600\ \text{L}$
HCl的物质的量:
$n(\text{HCl}) = c_{\text{HCl}} \cdot V_{\text{HCl}} = 0.01105 \cdot 0.00600 = 0.0000663\ \text{mol}$
步骤3:计算氨(NH₃)的物质的量
反应中HCl与NH₃按1:1反应,故:
$n(\text{NH₃}) = n(\text{HCl}) = 0.0000663\ \text{mol}$
步骤4:计算氮(N)的质量
每个NH₃分子含1个N原子,故:
$n(\text{N}) = n(\text{NH₃}) = 0.0000663\ \text{mol}$
氮的质量:
$m(\text{N}) = n(\text{N}) \cdot M_N = 0.0000663 \cdot 14.00 = 0.0009282\ \text{g} = 0.9282\ \text{mg}$
步骤5:计算原样品中的总氮含量
5.00mL肉样溶液中的氮含量为0.9282mg,定容后总体积为100.00mL,故原溶液中总氮含量:
$\text{总氮含量} = 0.9282\ \text{mg} \cdot \frac{100.00}{5.00} = 18.564\ \text{mg}$
步骤6:计算单位质量的氮含量
原肉样质量为8.00g,故:
$\text{挥发性盐基氮含量} = \frac{18.564\ \text{mg}}{8.00\ \text{g}} = 2.3205\ \text{mg/g} \approx 2.32\ \text{mg/g}$