题目
【题文】Ba(OH)2溶液中滴加NaHSO4溶液之后,溶液导电能力随滴入NaHSO4溶液体积变化曲线如图所示。力 A-|||-B-|||-、 C D-|||-_(1) V2-|||-(NaHS(O)_(4))/mL(1) AB段反应的离子方程式为_______。(2) C点对应的溶液呈_______ (填 “酸”、“ 碱” “中”)性。(3)D点对应的溶液中存在的离子主要是_______。(4)V1、V2的关系为_______。
【题文】Ba(OH)2溶液中滴加NaHSO4溶液之后,溶液导电能力随滴入NaHSO4溶液体积变化曲线如图所示。
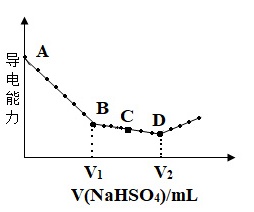
(1) AB段反应的离子方程式为_______。
(2) C点对应的溶液呈_______ (填 “酸”、“ 碱” “中”)性。
(3)D点对应的溶液中存在的离子主要是_______。
(4)V1、V2的关系为_______。

(1) AB段反应的离子方程式为_______。
(2) C点对应的溶液呈_______ (填 “酸”、“ 碱” “中”)性。
(3)D点对应的溶液中存在的离子主要是_______。
(4)V1、V2的关系为_______。
题目解答
答案
【答案】Ba2++OH-+H++SO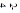 =BaSO4↓+H2O 碱 Na+、SO
=BaSO4↓+H2O 碱 Na+、SO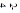 V1:V2=1:2
V1:V2=1:2
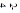 =BaSO4↓+H2O 碱 Na+、SO
=BaSO4↓+H2O 碱 Na+、SO V1:V2=1:2
V1:V2=1:2解析
【解析】
步骤 1:AB段反应的离子方程式
在AB段,Ba(OH)_2与NaHSO_4反应,生成BaSO_4沉淀和水,同时释放出Na^+和OH^-。反应的离子方程式为:Ba^{2+}+OH^{-}+H^{+}+SO=BaSO_4↓+H_2O。
步骤 2:C点对应的溶液的酸碱性
C点时,Ba(OH)_2与NaHSO_4恰好完全反应,生成BaSO_4沉淀和水,溶液中剩余的主要是Na^+和OH^-,因此溶液呈碱性。
步骤 3:D点对应的溶液中存在的离子
D点时,NaHSO_4过量,溶液中主要存在Na^+和SO,因为NaHSO_4在水中完全电离为Na^+、H^+和SO,而Ba(OH)_2与NaHSO_4反应生成BaSO_4沉淀和水,所以溶液中主要存在Na^+和SO。
步骤 4:V_1、V_2的关系
V_1表示Ba(OH)_2与NaHSO_4恰好完全反应时NaHSO_4的体积,V_2表示NaHSO_4过量时的体积。由于Ba(OH)_2与NaHSO_4反应的化学计量比为1:1,所以V_1:V_2=1:2。
步骤 1:AB段反应的离子方程式
在AB段,Ba(OH)_2与NaHSO_4反应,生成BaSO_4沉淀和水,同时释放出Na^+和OH^-。反应的离子方程式为:Ba^{2+}+OH^{-}+H^{+}+SO=BaSO_4↓+H_2O。
步骤 2:C点对应的溶液的酸碱性
C点时,Ba(OH)_2与NaHSO_4恰好完全反应,生成BaSO_4沉淀和水,溶液中剩余的主要是Na^+和OH^-,因此溶液呈碱性。
步骤 3:D点对应的溶液中存在的离子
D点时,NaHSO_4过量,溶液中主要存在Na^+和SO,因为NaHSO_4在水中完全电离为Na^+、H^+和SO,而Ba(OH)_2与NaHSO_4反应生成BaSO_4沉淀和水,所以溶液中主要存在Na^+和SO。
步骤 4:V_1、V_2的关系
V_1表示Ba(OH)_2与NaHSO_4恰好完全反应时NaHSO_4的体积,V_2表示NaHSO_4过量时的体积。由于Ba(OH)_2与NaHSO_4反应的化学计量比为1:1,所以V_1:V_2=1:2。